심장질환 검출을 위한 딥러닝 모델 기반 심전도 신호 재구성에 관한 연구
초록
애플워치, 갤럭시워치와 같은 스마트워치에서 취득하는 심전도 신호는 의료기관에서 측정하는 표준 12 리드 심전도 신호와 달리 단일 리드 신호만 취득하기 때문에 심장질환에 대한 정밀 진단에 어려움이 있다. 본 논문에서는 소수의 심전도 신호를 학습하여 표준 12리드 심전도 신호를 재구성하기 위해 LSTM. Bi-LSTM, GRU과 같은 시계열 기반의 단일 딥러닝 모델 유사도 결과를 비교한다. 실험 결과, 각 딥러닝 모델에서 재구성한 심전도 신호와 실제 심전도 신호간의 선형상관계수의 경우 LSTM모델은 0.793이며, Bi-LSTM모델은 0.928, GRU모델는 0.944로 출력되었다. 또한, RMSE의 경우 LSTM모델은 0.153이며, Bi-LSTM모델은 0.071, GRU모델는 0.07로 출력되었다. 따라서 소수의 심전도 신호로 이용하여 GRU 기반 딥러닝 모델을 통해 재구성한 표준 12리드 심전도 신호의 유사도가 가장 높게 나타내는 것을 확인하였다.
Abstract
With the rapidly increasing online data, recommender systems are becoming more important. Therefore, the growth of e-commerce data presents new challenges for storing and querying large amounts of data for online recommendation systems. However, there is little research on processing extensive online data to improve the performance of large-scale recommendation systems. This paper proposes a new graph data storage model for large-scale recommendation systems. Additionally, the proposed model includes a new type of index to quickly generate recommendation lists. We also conduct comparison experiments with existing data models and demonstrate that our distributed graph data model outperforms other data models, such as the relational data model, in large-scale recommendation systems.
Keywords:
electrocardiogram, lstm, bidirectional-lstm, gru, signals reconstructionⅠ. 서 론
웨어러블 디바이스로부터 측정되는 심전도 신호를 딥러닝 기술로 분석함으로써, 시공간적 제약 없이 심장질환을 조기 진단하고 예방하는 연구가 활발히 진행 중이다. 심전도 신호는 심장의 활동할 때 나타나는 전기적인 신호를 그래프로 기록한 것으로 심전도 신호의 한 주기는 심방의 탈분극에 의해 발생하는 P파, 심실의 탈분극에 의해 발생하는 QRS파, 그리고 심실의 재분극에 의한 T파의 특징점이 있다[1][2]. 또한, 심전도 신호는 측정 위치에 따라 6개의 사지 유도(Lead I, Lead II, Lead III, aVR, aVL, aVF)와 6개의 흉부 유도(V1~V6)로 표준 12 리드 심전도 신호를 측정할 수 있으며, 이를 분석하여 다양한 심장질환을 진단할 수 있다[3][4].
최근에는 애플워치, 갤럭시워치와 같은 웨어러블 디바이스 제품들이 상용화되어 일상생활에서 간편하게 심전도 신호를 측정할 수 있다[5]-[7]. 그러나, 웨어러블 디바이스를 이용한 심전도 신호는 단일 심전도 신호만을 측정할 수 있기 때문에, 표준 12 리드 심전도 신호를 이용한 진단 정확도에 비해 낮은 정확성을 나타낸다. 이에, 웨어러블 디바이스로부터 취득한 단일 심전도 신호를 이용하여 표준 12 리드 심전도 신호를 생성할 수 있는 기술에 대한 연구가 필요하다.
본 논문에서는 3개의 리드 신호(Lead I, II, III)를 이용하여 표준 12리드 심전도 신호를 재구성하고, 이를 위해 세 가지 시계열 딥러닝 모델인 LSTM, Bi-LSTM, GRU에 적용하여 각 모델의 재구성 성능을 비교하고 분석하는 것이다. 각 모델에 대해 Pearson 상관계수(PCC, Pearson Correlation Coefficient)와 평균 제곱근 오차(RMSE, Root Mean Square Error)를 사용하여 정량적인 성능 평가를 수행하였으며, 이를 통해 심전도 신호 재구성에 가장 적합한 딥러닝 모델을 도출하고자 한다. 먼저 실험에 필요한 데이터베이스 구성 과정에서 심전도 신호의 왜곡과 파형 변화를 최소화하기 위해 잡음제거 및 정규화 과정은 적용하지 않았다. 다음으로 동일한 환경에서 생성 유사도 결과를 비교하기 위해 시계열 딥러닝 모델은 단일 모델의 형태로 3개의 LSTM. Bi-LSTM, GRU 계층과 Batch normalization 계층, Dropout 계층 그리고 동일한 파라미터의 값으로 구성하였다[8]-[10]. 재구성한 심전도 신호와 원본 심전도 신호와의 유사도 비교는 평균 제곱근 오차(RMSE)와 피어슨 상관계수(PCC) 지표를 이용하였다. 실험 결과, 각 딥러닝 모델의 PCC의 경우 LSTM 모델은 0.793이며, Bi-LSTM 모델은 0.928, GRU 모델은 0.944로 출력되었다. 또한, 각 딥러닝 모델의 RMSE의 경우 LSTM 모델은 0.153이며, Bi-LSTM 모델은 0.071, GRU 모델은 0.07로 출력되었다. 따라서 GRU 기반 딥러닝 모델을 통해 재구성한 표준 12리드 심전도 신호의 유사도가 원본 심전도 신호와 가장 유사하게 생성되는 것을 확인하였다.
본 논문의 구성은 2장에서 생체신호 재구성을 위한 기존 연구에 대해 분석하고, 3장에서 표준 12 리드 재구성을 위해 본 논문에서 사용한 시계열 기반의 딥러닝 모델에 대해 설명한다. 4장에서 재구성된 신호에 대한 실험 결과를 분석하고, 끝으로 5장에서 결론을 맺는다.
Ⅱ. 관련 연구
웨어러블 기기에서 측정된 심전도 신호는 단일 리드의 심전도 신호로 심장질환 진단에 필요한 표준 12 리드 심전도 신호에 비해 정보가 부족한 문제가 있다. 이러한 문제점을 보완하고자 합성곱 신경망, 순환신경망, 적대적 생성 신경망 등 인공지능 모델을 이용하여 심전도 신호를 재구성하는 연구가 진행되고 있다. 본 장에서는 소수의 심전도 신호를 이용하여 표준 12 리드 심전도 신호를 재구성하기 위한 기존 연구에 대해 분석한다.
L. D. Wang et al.[11]은 Lead-I, II, V2를 입력하여 나머지 9개 리드를 재구성하는 합성곱 신경망 모델을 제안하였다. 데이터베이스는 PTB diagnostic ECG database이며, 3개의 리드 심전도 신호를 2차원 형태로 변환한 후 합성곱 신경망에 적용하였다. 실험 결과 합성곱 신경망 방법은 선형회귀법과 ANN 방법보다 높은 정확도를 보였으며, 처리 시간에서도 ANN 방법보다 93% 빠른 성능을 나타냈다. N. Dhahri et al.[12]는 딥러닝 모델의 파라미터 설정 문제를 해결하여 최적의 심전도 신호 재구성을 위해 유전 알고리즘(Genetic algorithm)을 LSTM 모델에 적용한 심전도 신호 재구성 시스템을 제안하였다. 데이터베이스 구성은 PTB Diagnostic ECG Database의 일부 데이터를 학습에 사용하였으며, 나머지를 검증에 활용하였다. 모델 성능 평가는 상관계수와 RMSE를 이용하여 유사도를 평가하였다. 실험 결과 재구성된 리드별 상관계수의 평균은 0.95이며, RMSE는 0.06을 나타냈다.
A. Kapfo et al.[13]는 리드 I, II, V2의 3개 독립 리드만을 입력으로 활용하여 12리드 ECG 전체를 재구성하는 방법을 제안하였다. 특히, 진단에 필요한 정보를 손실없이 복원하기 위해 DWT(Discrete Wavelet Transform)를 이용하여 다해상도로 변환하였으며, LSTM 기반 딥러닝 모델에 적용하였다. 모델 성능 평가는 상관계수와 WEDD(Wavelet Energy Diagnostic Distortion)를 이용하여 유사도를 평가하였다. 실험 결과, 상관계수의 평균은 0.98이며, WEDD는 21.02%를 나타냈다. G. W. Yoon et al.[14]은 단일 리드(Lead-I)만을 사용하여 흉부 리드(V1~V6)을 생성하는 적대적 생성 신경망 기반 딥러닝 모델을 제안하였다. 제안한 모델은 U-Net 기반 생성기(Generator)와 PatchGAN 판별기(Discriminator) 구조로 구성되어 있으며, 성능 평가는 FD(Fréchet Distance), MSE(Mean Squared Error)를 통해 평가하였다. 실험 결과, PTB-XL 데이터베이스에 대한 FD의 평균값은 11.321이며, MSE는 0.038을 나타냈다.
인공지능 모델 외에도 다양한 머신러닝 기법을 활용하여 심전도 신호를 재구성하는 연구가 진행되고 있다. S. Padhy et al.[15]은 SVD(Singular Value Decomposition) 방법을 통해 표준 12리드 신호를 생성하는 방법을 제안하였다. 입력 심전도 신호를 SVD를 통해 저차원 공간으로 투영한 후, 변환된 행렬을 학습하여 표준 12리드 신호를 재구성하였다. 각 리드 간의 상호 상관성(Interlead correlation)을 활용하여 선형적 특징을 생성하며, 리드별 상관계수가 0.9이상으로 높은 재현율을 나타냈다. P. Sindreu et al.[16]은 선형 회귀(Linear regression)가 주성분 분석 기반 방법을 이용하여 3개의 심전도 신호(lead I, II, V2)를 이용하여 신호 공간의 차원을 축소하고 주성분만을 이용해 나머지 리드 신호를 추정하였다. 재구성된 신호는 원본 심전도 신호와 높은 상관관계를 보였으나, 일부 리드 신호는 잡음이나 자세 변화에 따른 오차가 발생하였다. J. H. Lee et al.[17]은 사지 리드(Limb leads) 신호만을 이용하여 전흉부 리드(Precordial leads, V1~V6)를 재구성하기 위해 상태공간(State-space) 모델을 제안하였다. 기존의 선형회귀 기반 심전도 신호 재구성 방법의 시간적 특성이 반영되지 않은 문제점을 해결하기 위해 시간적 특성을 예측할 수 있는 Kalman Filter를 사용하여 정밀한 심전도 신호를 재구성하였다.
본 연구는 3개의 리드 신호를 사용하여 12리드 심전도 신호를 재구성하기 위해 LSTM, Bi-LSTM, GRU 모델을 각각 적용하고, 각 모델의 성능을 비교하여 최적의 모델을 선정하는 것을 목표로 하였다. 기존 연구들은 심전도 신호의 정밀한 재구성을 위해 다양한 딥러닝 모델 설계 방안을 제안하는 데 중점을 두었으나, 본 연구는 모델의 성능을 정량적으로 평가하는 방법을 통해 세 모델 간의 차별성과 장단점을 비교 분석하였다.
Ⅲ. 심전도 신호 재구성을 위한 시계열 기반 딥러닝 모델
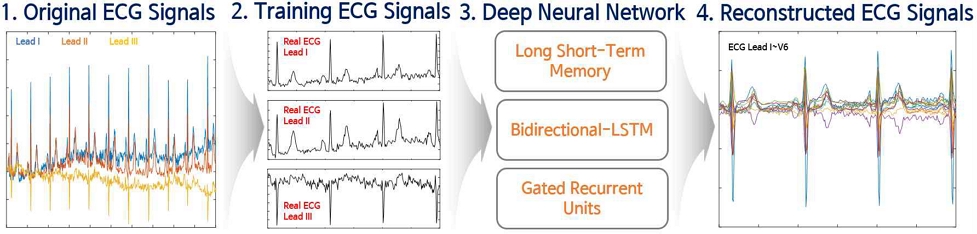
그림 1은 본 논문에서 제시한 심전도 신호 재구성 방법의 전체적인 흐름도이다. 먼저 입력된 원본 신호로부터 동일한 데이터 길이의 구간별로 학습, 검증, 실험 데이터로 분할한다. 다음으로 분할한 Lead I~III의 심전도 신호로 표준 12리드 심전도 신호를 재구성하기 위해 시계열 데이터에 강인한 순환신경망 기반 LSTM, Bi-LSTM, GRU 모델에 적용한다. 동일한 환경에서 생성 유사도 결과를 비교하기 위해 시계열 딥러닝 모델은 단일 모델의 형태로 각 3개의 LSTM. Bi-LSTM, GRU layer, Batch normalization layer, Dropout layer로 구성하였다. LSTM은 이전 정보를 오랫동안 저장하지 못하는 RNN의 문제점을 보완한 딥러닝 모델이다. 먼저, RNN은 일반 신경망에서 시계열 정보를 이용할 수 있는 개념이 추가된 신경망으로 은닉층에서 다시 자기 자신으로 돌아오는 가중치가 추가되어 이전의 정보를 현재의 시간에 이용할 수 있는 장점이 있다.
그러나 시퀀스가 길어질수록 기울기 값이 소실되는 문제로 초기에 입력된 정보가 출력 결과에 영향을 미치지 못하는 문제와 오버피팅 문제가 발생할 수 있으며 학습 시간이 오래 걸리는 단점이 있다. LSTM은 정보가 소실되는 장기 의존성 문제를 해결하기 위해 제안된 모델로 기존 RNN의 은닉층에 Memory cell이라 불리는 은닉층을 대체하여 장기 의존성 문제를 해결하였다.
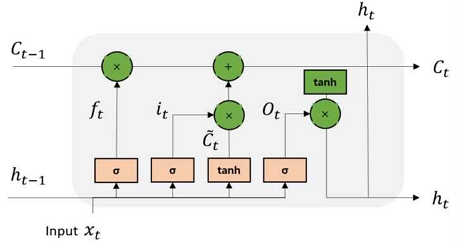
그림 2에서 보는 것과 같이 LSTM은 Input gate, output gate, Cell state, forget gate로 구성되어 있으며, 활성화 함수는 시그모이드 함수와 하이퍼볼릭 탄젠트 함수를 사용한다[12]. Forget gate는 Cell state에서 현재 정보의 제거 정도를 결정하며, Input gate는 현재 정보의 반영 정도, Output gate는 데이터의 출력을 결정한다. Cell state는 이전 Gate에서 삭제할 정보와 업데이트할 정보를 결정하면 Cell state update 과정을 진행한다. 즉 새로운 후보 계층은 이전의 Cell state를 새로운 Cell로 업데이트하기 위해 사용된다. LSTM에 대한 게이트와 출력에 대한 수식은 식 (1)~(6)과 같다.
| (1) |
| (2) |
| (3) |
| (4) |
| (5) |
| (6) |
ht-1는 이전 단계의 출력값, xt는 현재 단계의 입력값, W는 가중치를 의미한다. 게이트의 출력 결과인 ft가 1에 근접할수록 기울기가 소실되거나 발산하는 것을 방지할 수 있으며, 시간 변화에 따라 기울기가 오래 지속되는 것으로 판단할 수 있다.
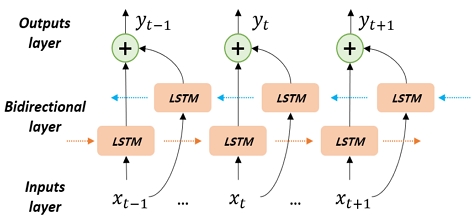
다음으로 Bi-LSTM은 시계열 데이터를 효과적으로 처리하는 데 널리 사용되는 LSTM(Long Short-Term Memory) 모델의 확장 구조로, 양방향 시계열 데이터를 동시에 학습할 수 있도록 설계되었다. LSTM은 현재 시점의 예측을 위해 과거의 정보만을 고려하지만, Bi-LSTM은 과거뿐만 아니라 미래의 정보까지도 함께 활용할 수 있다. Bi-LSTM은 그림 3과 같이 두 개의 LSTM 층을 병렬적으로 구성하여 하나는 입력 시퀀스를 정방향으로, 다른 하나는 역방향으로 처리한다. 각 시점의 출력은 이 두 방향의 hidden state를 결합(Concatenate)하여 최종적인 벡터를 생성한다. 이로인해 시점 t에서의 입력에 대해 과거 정보와 미래 모든 정보를 고려하기 때문에 보다 정교한 특징 추출이 가능하다. 특히 심전도 신호와 같은 생체신호는 패턴이 미세하고 개별 파형 간 시간적 관계가 중요한 특성을 가지므로, 이러한 양방향 데이터 처리는 심전도 신호의 패턴 이해와 생성을 위해 효과적인 접근 방식이다.
그러나 Bi-LSTM은 실시간 처리의 어려움이다. 미래의 정보가 필요한 구조적인 특성으로 인해 학습에 필요한 입력 시퀀스 전체 데이터가 확보된 후, 모델의 예측이 가능하므로 실시간 데이터 처리에는 적합하지 않다. 또한, 정방향과 역방향 두 개의 LSTM 네트워크를 사용하기 때문에 메모리 사용량과 계산량이 증가하고, 학습 시간이 길어지는 문제가 발생한다. 이로 인해 하드웨어 리소스가 제한된 환경에서는 모델 최적화나 경량화에 관한 연구가 필요하다. 또한 학습 파라미터가 많아지기 때문에 학습 데이터가 충분하지 않을 경우 과적합의 위험도 존재한다.
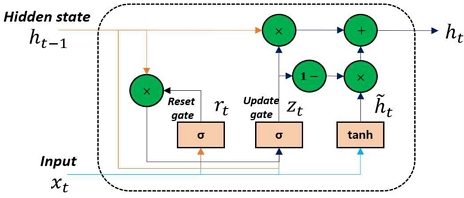
끝으로 GRU(Gated Recurrent Unit)는 순환신경망의 변형 모델로 시계열 데이터를 학습하는 과정에서 발생하는 장기 의존성 문제를 해결하기 위해 개발되었다. LSTM의 경우 장기 의존성 문제를 해결하기 위해 기존의 순환신경망보다 더 많은 파라미터를 요구하기 때문에 데이터가 충분하지 않을 경우 과적합 문제가 발생한다. GRU 모델은 과적합 문제를 해결하기 위해 LSTM의 구조를 개선한 모델로 input gate와 forget gate를 융합하여 연산 효율성을 높이기 위한 단순한 구조를 가지도록 설계되었다. LSTM에서는 출력, 입력, 망각으로 구성된 3개의 게이트로 구성되어 있지만, GRU는 그림 4와 같이 LSTM의 망각 게이트와 입력 게이트를 하나로 융합한 업데이트 게이트와 새로운 리셋 게이트로 2개의 게이트로 구성되어 있다. GRU의 특징으로는 LSTM에 비해 구조가 간단하고 적은 파라미터 수를 이용하기 때문에 학습 속도가 빠르며, 더 적은 메모리를 요구하는 특징이 있다. 특히 GRU는 실시간 예측 시스템과 같은 제한된 자원 환경에서 유용하게 사용된다고 알려져 있다.
따라서, LSTM, Bi-LSTM, GRU는 시계열 데이터를 효과적으로 처리할 수 있도록 고안된 구조로, 본 논문에서는 심전도 신호 재구성에 가장 적합한 모델을 도출하기 위한 각 모델의 성능을 비교에 중점을 두었다. LSTM은 장기 의존성 정보를 반영할 수 있으나, 구조가 복잡하고 연산량이 많다. Bi-LSTM은 입력 데이터를 양방향으로 처리해 정확도를 높일 수 있지만, 실시간 처리에는 한계가 있다. GRU는 상대적으로 간단한 구조로 학습 속도가 빠르며, 연산 효율성이 높아 실시간 응용에 적합하다.
Ⅳ. 실험결과 및 분석
본 논문에서 사용된 데이터베이스는 PhysioNet에 공개되어 있는 PTB-XL 내에 30명의 표준 12리드 심전도 신호를 사용하였으며, 심박수/나이/성별 등의 정보가 포함되어 있다. 심전도 신호의 sampling rate는 100Hz로 10초 동안 측정되었다[18]. 즉, 각각의 심전도 신호의 길이(Sampling)는 1,000 sampling으로 표준 12리드 심전도 신호로 구성되어 있다. 전체 심전도 신호의 길이에서 심전도 측정 시 발생하는 전력선 잡음, 근 잡음, 전극 접촉 잡음 등으로 인해 시작점으로부터 100 sampling은 제거하였다. 따라서, 전체 데이터로부터 학습 데이터는 101~400 sampling, 검증 데이터는 401~700 sampling, 재구성된 심전도 신호와 유사도를 비교하기 위한 실험 데이터는 나머지 701~1,000 sampling을 사용하였다. 재구성된 심전도 신호와 실제 심전도 신호 간의 유사도를 정량적으로 평가하고 다양한 관점에서 비교하기 위해 RMSE와 PCC를 이용하였다[19][20].
| (7) |
| (8) |
먼저 RMSE는 식 (7)과 같이 모델의 예측값과 실제값 간의 차이를 제곱한 후 평균을 구하고 다시 제곱근을 연산한 결과이며, 오차의 크기와 분포를 나타내기 때문에 값이 작을수록 예측값이 실제값과 유사하는 것을 의미한다. PCC는 실제 신호와 예측 신호 간의 선형적인 관계를 나타내는 지표로 식 (8)을 통해 상관계수 r값을 연산할 수 있으며, r의 범위는 –1~1사이이다. 이러한 평가지표를 통해 시계열 기반의 딥러닝 모델 성능을 정량적으로 비교하며, 재구성한 심전도 신호와 실제 심전도 신호 간의 유사성을 평가하였다.
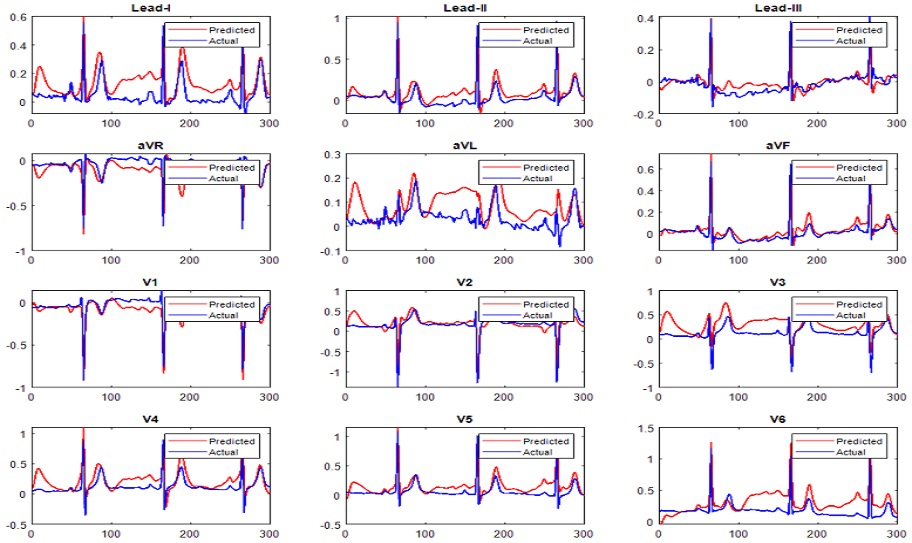
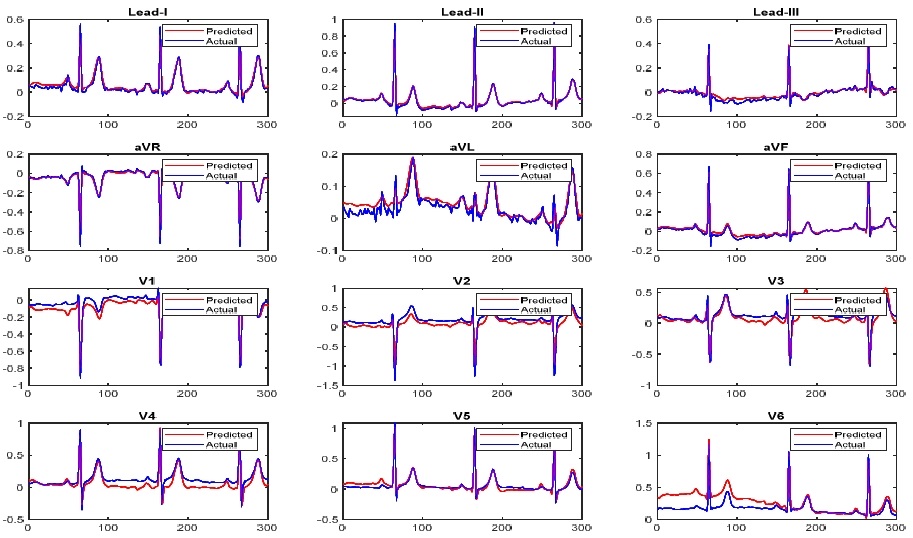
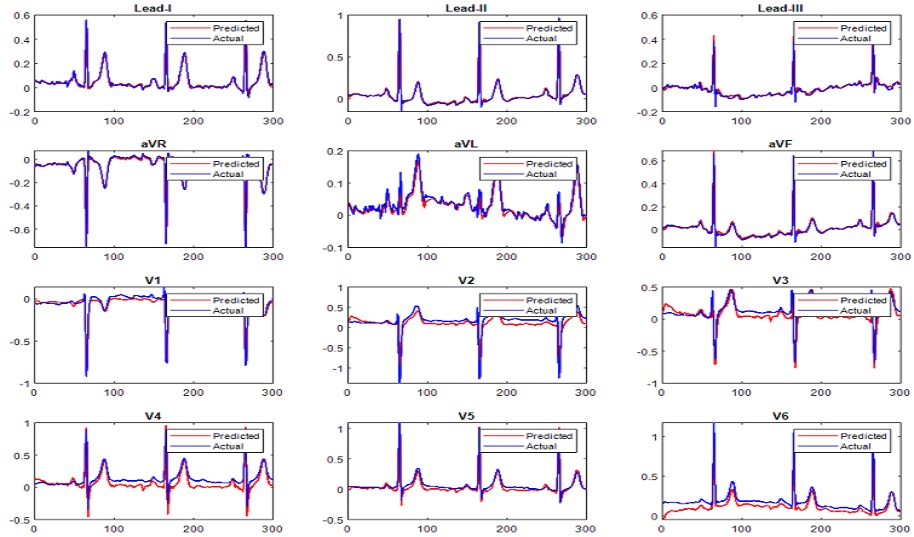
실험 결과, LSTM의 RMSE는 0.153, Bi-LSTM은 0.071, GRU는 0.070으로 나타났다. 이를 통해 Bi-LSTM과 GRU가 LSTM에 비해 0.083의 차이로 현저히 낮은 오차를 보였으며, GRU는 가장 낮은 RMSE를 나타내 실제 심전도 신호와 재구성한 심전도 신호의 유사성에서 가장 우수한 성능을 나타냈다. 다음으로, PCC의 경우, LSTM의 상관계수는 0.793이며, Bi-LSTM과 GRU는 각각 0.928과 0.944를 기록하였다. 특히 GRU는 높은 상관도를 통해 실제 심전도 신호와 유사한 심전도 신호 재구성의 가능성을 확인하였다. 그림 5~7은 각 모델에서 재구성한 표준 12 리드 심전도 신호 결과로 파란 선은 실제 심전도 신호이며, 빨간 선은 재구성한 심전도 신호를 의미한다.
종합적으로 심전도 신호 재구성에 대한 유사성 평가 결과는 각 모델의 구조적 특성의 차이임을 확인할 수 있었다. 각 모델의 파라미터 수를 확인하였을 때, LSTM의 파라미터의 수는 51.8k이며, Bi-LSTM은 143.6k, GRU는 39k를 사용하였다. 이에, LSTM은 시계열 정보를 장기적으로 유지하는 데 적합하지만, 상대적으로 많은 파라미터와 복잡한 구조로 인해 학습률에서 제한이 발생하여 다른 시계열 기반의 딥러닝 모델에 비해 낮은 유사성을 나타냈다.
반면, Bi-LSTM은 과거와 미래 정보를 모두 고려할 수 있는 양방향 구조를 가지므로 시계열 신호의 전후 맥락을 동시에 학습할 수 있어 정밀한 심전도 신호의 재구성에 대한 가능성을 확인하였다. GRU는 LSTM에 비해 구조가 간단하면서도 유사한 정보 보존 능력을 지니고 있기 때문에, 계산 효율성과 학습 성능에서 우수한 성능을 나타냈다. 따라서, 본 연구에서는 GRU가 가장 적은 파라미터 수를 사용하면서 낮은 오차를 나타냄으로써, 심전도 신호 재구성에 있어 가장 효과적인 모델로 확인하였다.
Ⅴ. 결 론
사용자가 일상생활에서 스마트워치를 이용하여 취득하는 심전도 신호는 의료기관에서 측정하는 표준 12 리드 심전도 신호와 달리 단일 리드 신호만 취득하기 때문에 심장질환에 대한 정밀 진단에 어려움이 있다. 이러한 문제를 해결하기 위해 소수의 심전도 신호로 표준 12 리드 신호를 재구성할 수 있는 연구가 진행되고 있다. 그러나 기존의 인공지능 모델 또는 머신러닝 기법을 이용해 심전도 신호를 재구성하는 연구는 시계열 데이터에 대한 시간적 정보와 시간 의존성을 이해하는데 어려움이 있다. 또한, 데이터의 전체 분포를 학습하기 때문에 고품질의 원본 신호와 유사한 데이터 생성은 가능하지만, 다양한 패턴의 데이터를 생성하지 못하는 문제점이 있다.
이에, 본 논문에서는 소수의 심전도 신호를 학습하여 표준 12 리드 심전도 신호를 재구성하기 위해 LSTM. Bi-LSTM, GRU과 같은 시계열 기반의 단일 딥러닝 모델을 분석하고 이를 이용하여 심전도 신호를 재구성하였다. 재구성한 심전도 신호를 정량적으로 평가를 위해 평균 제곱근 오차와 피어슨 상관계수의 결과를 통해 원본 심전도 신호와 유사도 결과를 비교하였다. 실험 결과, GRU가 LSTM과 Bi-LSTM보다 가장 적은 파라미터 수를 사용하면서도 가장 높은 유사도 결과를 나타냄으로써, 심전도 신호 재구성을 위한 가장 효과적인 모델로 확인하였다. 향후에는 실제 표준 12 리드 심전도 신호와 재구성한 표준 12 리드 심전도 신호를 이용하여 부정맥 신호 검출 성능 비교에 관한 연구를 진행할 계획이다.
Acknowledgments
본 연구는 과학기술정보통신부의 재원으로 정보통신기획평가원의 지원을 받아 수행된 정보통신ㆍ방송 기술개발 사업(No. RS-2022-000317, RS-2025-002219190)의 지원을 받아 수행된 연구임
References
-
M. G. Kim and S. B. Pan, "A Study on User Recognition based on 1D Dilated Convolution using ECG Signal", Journal of KIIT, Vol. 19, No. 10, pp. 99-104, Oct. 2021.
[https://doi.org/10.14801/jkiit.2021.19.10.99]

-
M. G. Kim, C. Choi, and S. B. Pan, "Ensemble networks for user recognition in various situations based on electrocardiogram", IEEE Access, Vol. 8, pp. 36527-36535, Feb. 2020.
[https://doi.org/10.1109/ACCESS.2020.2975258]

-
H. L. Kennedy, "Ambulatory (Holter) electrocardiography technology", Cardiology Clinics, Vol. 10, No. 3, pp. 341-359, Aug. 1992.
[https://doi.org/10.1016/S0733-8651(18)30218-2]

-
J. P. DiMarco and J. T. Philbrick, "Use of ambulatory electrocardiographic (Holter) monitoring", Annals of internal medicine, Vol. 113, No. 1, pp. 53-68, Jul. 1990.
[https://doi.org/10.7326/0003-4819-113-1-53]

-
A. Samol, K. Bischof, D. Pascut, M. Wiemer, and S. Kaese, "Recording of bipolar multichannel ECGs by a smartwatch: modern ECG diagnostic 100 years after Einthoven", Sensors, Vol. 19, No. 13, Jun. 2019.
[https://doi.org/10.3390/s19132894]

-
A. Samol, et al., "Patient directed recording of a bipolar three-lead electrocardiogram using a smartwatch with ECG function", Journal of Visualized Experiments, Dec. 2019.
[https://doi.org/10.3791/60715]

-
M. G. Kim and J. H. Jung, "A Study on Arrhythmia Classification Using Multi-Stream CNN Based on Variational Mode Decomposition", Journal of KIIT, Vol. 23, No. 8, pp. 19-26, Aug. 2025.
[https://doi.org/10.14801/jkiit.2025.23.8.19]

-
S. Hochreiter and J. Schmidhuber, "Long Short-Term Memory", Neural Computation, Vol. 9, No. 8, pp. 1735-1780, Nov. 1997.
[https://doi.org/10.1162/neco.1997.9.8.1735]

-
M. Schuster and K. K. Paliwal, "Bidirectional recurrent neural networks", IEEE Transactions on Signal Processing, Vol. 45, No. 11, pp. 2673-2681, Nov. 1997.
[https://doi.org/10.1109/78.650093]

-
K. Cho, et al., "Learning phrase representations using RNN encoder-decoder for statistical machine translation", arXiv preprint arXiv:1406.1078, , Jun. 2014.
[https://doi.org/10.48550/arXiv.1406.1078]

-
L. D. Wang, et al., "A novel method based on convolutional neural networks for deriving standard 12-lead ECG from serial 3-lead ECG", Frontiers of Information Technology & Electronic Engineering, Vol. 20, No. 3, pp. 405-413, Apr. 2019.
[https://doi.org/10.1631/FITEE.1700413]

-
N. Dhahri, N. Majdoub, T. Ladhari, A. Sakly, and F. Msahli, "Reconstruction of 12-lead ECG with an optimized LSTM neural network", 2022 IEEE 21st International Conference on Sciences and Techniques of Automatic Control and Computer Engineering, Sousse, Tunisia, pp. 320-324, Dec. 2022.
[https://doi.org/10.1109/STA56120.2022.10019143]

-
A. Kapfo, S. Datta, S. Dandapat, and P. K. Bora, "LSTM based synthesis of 12-lead ECG signal from a reduced lead set", SPICES 2022 - IEEE International Conference on Signal Processing, Informatics, Communication and Energy Systems, Thiruvananthapuram, India, pp. 296-301, Mar. 2022.
[https://doi.org/10.1109/SPICES52834.2022.9774204]

-
G. W. Yoon, H. C. Seo, C. Kyungmin, K. Hannah, and S. Joo, "Chestlead generation with single-lead", 2022 Computing in Cardiology, Tampere, Finland, Sep. 2022.
[https://doi.org/10.22489/CinC.2022.075]

-
S. Padhy and S. Dandapat, "Synthesis of 12-lead ECG from a reduced lead set using singular value decomposition", 2015 IEEE Power, Communication and Information Technology Conference, Bhubaneswar, India, Oct. 2015.
[https://doi.org/10.1109/PCITC.2015.7438183]

-
P. Sindreu, I. Mansergas, D. Cano, and O. Casas, "Standard 12-lead ECG synthesis from homecare wearable measures", 2023 IEEE Int. Workshop Metrol. Ind. 4.0. & IoT, Brescia, Italy, Jun. 2023.
[https://doi.org/10.1109/MetroInd4.0IoT57462.2023.10180025]

-
J. H. Lee, M. K. Kim, and J. K. Kim, "Reconstruction of precordial lead electrocardiogram from limb leads using the state-space model", IEEE Journal of Biomedical and Health Informatics, Vol. 20, No. 3, pp. 818-828, May 2016.
[https://doi.org/10.1109/JBHI.2015.2415519]

- PhysioNet PTB-XL, a large publicly available electrocardiography dataset, https://physionet.org/content/ptb-xl/1.0.3/, . [accessed: Jul. 02, 2025]
-
J. H. Joo, G. H. Joo, Y. J. Kim, M. N. Jin, J. B. Park, and H. S Im, "Twelve-Lead ECG reconstruction from single-lead signals using generative adversarial networks", Medical Image Computing and Computer Assisted Intervention, Vancouver, BC, Canada, pp. 184-194, Oct. 2023.
[https://doi.org/10.1007/978-3-031-43990-2_18]

-
J. Benesty, J. Chen, Y. Huang, and I. Cohen, "Pearson correlation coefficient", Noise reduction in speech processing, Vol. 2, pp. 1-4, 2009.
[https://doi.org/10.1007/978-3-642-00296-0_5]


2011년 2월 : 조선대학교 제어계측로봇공학과(공학사)
2013년 2월 : 조선대학교 제어계측공학과(공학석사)
2019년 8월 : 조선대학교 제어계측공학과(공학박사)
2019년 9월 ~ 2023년 5월 : 조선대학교 IT연구소 연구교수
2023년 12월 ~ 현재 : 씨에스에스 기업부설연구소 연구원
관심분야 : 생체인식, 영상처리, 인공지능, 패턴인식

2015년 9월 ~ 2018년 12월 : 조선대학교 IT융합신기술연구센터 연구원
2019년 2월 : 조선대학교 IT융합학과(공학박사)
2019년 3월 ~ 2025년 2월 : 조선대학교 인공지능 헬스케어 연구센터 연구교수
2025년 3월 ~ 현재 : 을지대학교 빅데이터인공지능학과 조교수
관심분야 : 생체신호 취득 시스템, 질병예측, 인공지능