커스텀 모델 설계를 통한 QQ 모델 예측 정확도 향상
초록
자기공명영상을 활용한 뇌 조직 내 산소추출률의 정량적 계산은 뇌 활성도 평가 및 질환 진단에 있어 중요한 지표로 활용된다. 본 연구에서는 산소추출률 측정을 위한 QQ 모델의 다섯 가지 생리학적 파라미터(S0, R2, Y, v, χnb)를 동시에 예측하기 위해 커스텀 3차원 합성곱 신경망 회귀 모델을 제안한다. 제안한 모델은 1개의 입력 계층, 3개의 Conv3D 및 LeakyReLU 활성화 함수가 적용된 은닉 계층, 1개의 출력 계층으로 구성되며, 간결한 구조를 통해 학습 효율성과 해석 가능성을 확보하였다. 제안한 모델에 대해 자기공명영상 기법에서 신호 감쇄 및 자화율 데이터를 활용한 실험 결과, 주요 채널(Y)에서는 기존 방식과 유사한 수준의 성능을 보였고, 나머지 네 개 파라미터에서는 예측 정확도가 향상되어 다채널 회귀 문제에서 우수한 성능을 입증하였다.
Abstract
Quantitative estimation of the Oxygen Extraction Fraction (OEF) within brain tissue using Magnetic Resonance Imaging (MRI) is a key indicator for assessing brain activity and diagnosing neurological disorders. We propose a custom 3-dimensional convolutional neural network regression model to simultaneously predict 5 physiological parameters(S0, R2, Y, v, χnb) of the QQ model used for OEF measurement. The model consists of 1 input layer, 3 hidden layers with Conv3D operations and LeakyReLU activation, and 1 output layer, ensuring training efficiency and interpretability. Experimental results using MRI signal decay and susceptibility data show that the proposed model performs comparably to existing methods on the primary channel(Y) and achieves improved prediction accuracy for the other 4 parameters, validating its superior performance in multi-channel regression tasks.
Keywords:
QQ model, brain MRI, 3D convolution, cosine annealing scheduler, regressionⅠ. 서 론
뇌 질환은 전 세계적으로 주요한 사망 원인 중 하나로, 조기 진단 및 치료가 환자 생존율과 삶의 질에 직접적인 영향을 미친다[1]. 뇌의 기능적 이상을 진단하기 위해서는 뇌 조직 내 산소 대사 상태를 정량적으로 평가할 수 있는 지표가 필요하며, 이에 따라 산소추출률(OEF, Oxygen Extraction Fraction)은 중요한 바이오마커로 활용된다. OEF는 뇌 혈류를 통해 공급된 산소 중 실제로 조직에서 사용된 비율을 나타내며, 뇌의 대사활성 및 병리적 변화를 반영할 수 있다.
기존에는 양전자 방출 단층촬영(Positron emission tomography)을 통해 OEF를 측정하는 방법이 일반적이었으나, 고비용과 방사선 노출, 낮은 공간 해상도 등의 한계가 존재하였다. 이러한 점을 극복하기 위해 비침습적이고 고해상도의 자기공명영상(MRI, Magnetic Resonance Imaging)을 기반으로 한 다양한 OEF 추정 기법이 제안되었다. 그 중 QSM(Quantitative Susceptibility Mapping)과 qBOLD(quantitative Blood Oxygenation Level Dependent)를 통합한 QQ(QSM+qBOLD) 모델은 별도의 생리학적 가정 없이 OEF를 정량화할 수 있다는 점에서 높은 유연성과 활용성을 보인다.
최근에는 QQ 모델 기반의 OEF 예측 정확도를 높이기 위해 다양한 딥러닝 모델이 도입되고 있으며, 특히 2D CNN(Convolutional Neural Network) 및 LSTM(Long Short-Term Memory) 구조를 활용한 연구들이 활발히 진행되어 왔다[2][3]. 그러나 이러한 접근 방식은 MRI의 3차원 구조를 온전히 반영하지 못하고, OEF 예측을 위한 특정 채널에 과도하게 초점을 맞추는 경향이 있어 다채널 예측의 정밀도가 낮은 한계가 존재한다.
본 연구에서는 3D CNN 구조를 기반으로 커스텀 변환한 OEF 예측 모델을 제안하며, 기존 연구와 달리 Batch Normalization 및 Dropout을 제거한 간결한 구조를 통해 학습 안정성과 해석 가능성을 높이고자 한다. 제안된 모델은 1개의 입력 계층과 3개의 Conv3D 은닉 계층, 1개의 Conv3D 출력 계층으로 구성되며, 모든 은닉 계층에는 LeakyReLU 활성화 함수를 적용하였다. 입력 데이터는 MRI 촬영 설정한 에코타임(TE, Echo Time)별 신호 감쇄값(8채널)과 자화율(1채널)로 이루어진 총 9채널이며, 출력은 OEF를 포함한 총 5개의 QQ 모델 변수(S0, R2, Y, v, χnb)로 구성된다. 본 모델은 PyTorch로 구현되었으며, Cosine annealing 기반 학습률 스케줄러와 Early stopping 기법을 도입하여 학습의 효율성과 일반화 성능을 동시에 확보하였다. 성능 분석을 위한 실험은 총 17명의 환자로부터 수집된 뇌 MRI 데이터를 활용하여 수행되었다.
본 논문의 구성은 다음과 같다. 2장에서는 관련 연구를 요약하며, 3장에서는 제안하는 커스텀 3차원 합성곱 신경망 회귀 모델을 이용해 OEF 예측하는 과정을 구체적으로 설명한다. 4장에서는 학습 결과에 따른 실험 결과와 평가 정확도를 제시하며, 마지막으로 5장에서 본 연구의 결론을 정리한다.
Ⅱ. 관련 연구
OEF는 뇌 조직의 대사 상태와 활성화 정도를 반영하는 중요한 생체지표로, 이를 정확히 계산하는 것은 뇌 질환의 조기 진단과 치료에 있어 핵심적인 역할을 한다. OEF를 예측하기 위한 다양한 접근법이 제안되었으며, 대표적인 모델로는 QUIXOTIC[4], qBOLD[5], QSM[6], 그리고 이들을 통합한 QQ[7] 모델이 있다.
2.1 qBOLD 및 QSM
qBOLD 모델은 MRI 데이터를 기반으로 혈액 산소포화도 변화에 따른 신호 감쇠를 모델링하여 OEF를 예측하는 기법이다. qBOLD는 MRI 데이터를 직접 활용할 수 있는 실용적 장점이 있으나, 혈류가 일정하다는 전제가 요구되어 실제 환경에서는 예측 정확도가 낮아질 수 있다. 최근에는 qBOLD의 한계를 극복하고자 Radiomics 분석과 결합하여 뇌 조직 손상 예측을 강화하거나, 약리적 자극(예: 아세타졸아마이드)에 따른 혈류 변화 민감도를 높이는 방향으로 발전하고 있다[8][9].
QSM은 조직 내 자기 감수성(Susceptibility)을 정량화하여 혈액 내 산소 농도 및 철분 농도를 분석하는 모델이다. 특히 정맥 산소포화도와 같은 주요 생리 지표를 추정할 수 있어 뇌 질환 연구에 유용하지만, 자기 감수도 변화에 매우 민감하고 잡음에 취약하다는 한계가 존재한다. 최근 QSM 연구에서는 딥러닝 기법을 적극 도입하여 정확도와 잡음 강건성을 향상시키고 있으며, 구체적으로 물리 기반 딥러닝을 활용한 MoDL-QSM 모델[10], 데이터 일관성을 높인 End-to-end 방식의 NeXtQSM[11], 그리고 개인 맞춤형 Unsupervised 딥러닝 기반 INR-QSM 모델[12] 등이 활발히 연구되고 있다
이러한 발전에도 불구하고 qBOLD 모델과 QSM은 여전히 특정 생리학적 가정에서만 정확한 결과를 보장할 수 있는 제약이 있으며[7], 특히 낮은 신호대잡음비(SNR) 조건에서는 여전히 한계를 보이고 있다.
2.2 QQ 모델
QQ 모델[7]은 QSM과 qBOLD를 결합하여 양자의 장점을 통합한 모델로, 별도의 생리학적 가정 없이도 OEF를 계산할 수 있도록 설계되었다. QQ 모델은 잡음 민감성 개선, 다양한 조건에서 활용 가능성, 효율성과 같은 강점을 갖는다. 즉, QSM과 qBOLD의 상호 보완적 특성을 통해 잡음에 대한 민감도를 줄였고, 특정 생리 조건에 의존하지 않고 다양한 환경에서 적용 가능하다. 또한, QSM의 자기 감수성과 qBOLD의 산소포화도 신호를 융합하여 정교한 OEF 계산 가능하여 효율적이다.
이 모델은 정맥 산소포화도(Y), 정맥 혈액량(v), 조직의 BOLD(Blood Oxygenation Level Dependent)효과를 제외한 횡이완계수(R2), TE 0에서의 신호 강도(S0), 비혈류 물질의 자화율(χnb) 등 총 5개의 파라미터를 기반으로 OEF를 계산한다. 이러한 특성 덕분에 최근에는 QQ 모델을 기반으로 한 딥러닝 접근법이 활발히 연구되고 있다.
2.3 딥러닝과 QQ 모델
최근에는 QQ 모델과 딥러닝 기술을 결합하여 OEF 예측 정확도를 향상하려는 시도가 활발히 이루어지고 있다. 예를 들어 LSTM[2], DNN[3], GRU[13] 기반의 다양한 신경망 모델들이 QQ 입력 변수와 출력 사이의 복잡한 비선형 관계를 학습하여 높은 예측 성능을 보이고 있다. 이러한 모델들의 경우에 기존 수작업 기반 모델링 기법보다 빠르고 정밀하며, 잡음에도 상대적으로 강인한 특징을 지닌다. 특히, 기존 연구에서는 2D 기반의 LSTM 또는 CNN 모델이 주로 사용되었으며, 이 경우 MRI의 3차원 공간 정보를 완전히 활용하지 못한다는 한계가 있다. 이를 보완하기 위한 시도로 최근에는 Conv3D 기반의 QQ-Net[14]이 제안되었으며, 이 모델은 3D U-Net 구조를 활용하여 QQ 모델 기반 OEF 예측의 정확도와 재구성 속도를 향상시켰다. 하지만 여전히 대부분의 기존 연구는 OEF 계산에 활용되는 산소포화도(Y) 채널 하나에만 집중하고 있으며, 정맥 혈액량(v), 신호 강도(S0), 조직 횡이완계수(R2), 자화율(χnb) 등 다른 출력 채널에 대한 예측 성능은 상대적으로 낮은 편이었다. 본 논문에서는 이러한 한계를 극복하기 위해 보다 간결하고 경량화된 커스텀 3D CNN 구조를 설계하고, 다채널 출력 전반에 대한 예측 안정성과 정확도를 동시에 확보하는 데 초점을 맞추었다.
Ⅲ. 커스텀 모델 설계를 통한 QQ 기반 산소추출률의 예측 정확도 향상 방법
본 장에서는 QQ 모델 기반의 OEF 예측을 위한 커스텀 3차원 합성곱 신경망(3D CNN) 모델의 설계 및 구현 과정을 기술한다. 제안하는 모델은 9채널 입력 데이터를 기반으로 5채널 출력을 생성하며, 정맥 산소포화도(Y)를 포함한 QQ 모델의 파라미터를 동시에 예측하는 구조로 구성되어 있다.
3.1절에서는 전체 Conv3D 아키텍처의 구조와 각 계층의 역할을 설명하며, 3.2절에서는 학습률 스케줄링을 위한 Cosine annealing scheduler의 적용 방법을 다룬다. 3.3절에서는 QQ 모델의 수학적 정의와 함께 본 연구에서 적용한 ROI 처리 방식 및 전처리 전략을 기술한다. 마지막으로 3.4절에서는 PyTorch로 구현된 실제 커스텀 3D CNN 모델 구조를 상세히 설명한다.
3.1 3D CNN 구조
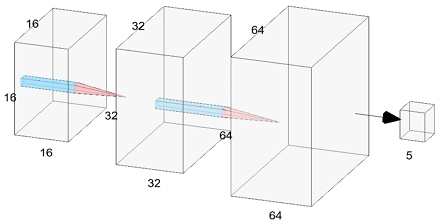
MRI는 본질적으로 3차원 볼륨 데이터를 포함하고 있으며, 슬라이스 간의 공간적 연속성을 유지하는 것이 신경망 학습에 중요한 요소로 작용한다. 기존의 2D CNN 기반 접근법은 각 슬라이스를 독립적으로 처리해야 하기 때문에, 깊이(Z-axis) 방향의 구조적 정보를 활용하기 위해 별도의 전처리 과정(예: 슬라이스 스태킹, 평균화 등)이 필요하였다. 반면, 3D CNN은 그림 1과 같이 입력 데이터를 3차원 볼륨 형태 그대로 처리함으로써 이러한 전처리 없이도 전체 공간 구조를 자연스럽게 반영할 수 있으며, 슬라이스 간의 연속적 특징까지 효과적으로 학습할 수 있다[15].
3.2 Cosine annealing 기반 학습률 스케줄링
딥러닝 모델의 학습 안정성과 일반화 성능은 학습률 설정에 큰 영향을 받는다. 특히 고정된 학습률을 사용하는 경우, 학습 초기에는 빠른 수렴이 가능하나 후반부에서는 손실 함수의 세밀한 최적화가 어렵고, 과적합 발생 가능성도 높아진다. 이를 개선하기 위해 본 연구에서는 Cosine annealing[16] 기반의 학습률 스케줄링 기법을 도입하였다.
Cosine annealing 방식은 학습률을 코사인 함수를 따라 점진적으로 감소시키는 전략으로, 학습 후반으로 갈수록 미세한 조정이 가능하도록 설계된다. 또한, 초기 학습 단계에서는 학습률을 선형으로 증가시키는 Warm-up 구간을 추가함으로써, 불안정한 가중치 초기화를 방지하고 안정적인 수렴 경로를 유도할 수 있다.
해당 스케줄링 기법은 Warm-up, 주기적 감소, 감쇠 계수 등의 조합을 통해 모델이 과적합 없이 최적화될 수 있도록 유도하며, 특히 반복적인 학습 주기(Cycle)를 통해 새로운 탐색과 세밀한 수렴을 균형 있게 달성할 수 있는 장점이 있다.
본 연구에서는 이러한 Cosine annealing 기반 스케줄링 전략을 학습 과정 전반에 걸쳐 적용하여, 모델이 초기에는 충분히 빠르게 수렴하고, 후반부에는 일반화 성능을 극대화할 수 있도록 유도하였다.
3.3 QQ 모델 파라미터 예측
OEF 예측을 위한 QQ 모델은 생리 모델인 QSM과 qBOLD를 통합한 접근 방식으로, 다음 식 (1)과 같이 정의된다.
| (1) |
식 (1)은 QQ 모델이 최적화하려는 손실 함수(Loss function)를 나타내며, QSM 및 qBOLD 기반의 신호 예측 결과와 실제 측정값 사이의 차이를 최소화하는 방향으로 파라미터를 추정한다. 여기서 최적화 대상은 총 5개의 생리학적 변수이다.
w는 QSM 항의 가중치이며, λ는 정규화 항의 가중치를 의미한다. FQSM과 SqBOLD는 각각 QSM과 qBOLD 모델의 신호 예측 함수이며, 실제 측정된 자화율 및 mGRE 신호와의 차이를 최소화하는 방식으로 동작한다. 해당 수식은 J. Cho et al.[7]의 연구에서 제안된 QQ 모델과 이를 활용한 Kim and Lee[3]의 손실 함수 구성에 근거하고 있다.
본 연구에서 사용된 데이터는 기존에 제안된 CAT(Cluster Analysis of Time-evolution) 기반 방법에서 활용된 QQ 모델 관련 데이터셋을 참고하여 구성되었다[17]. 해당 데이터셋에는 8개의 에코 타임에서 측정된 mGRE 신호, 자화율 정보, 그리고 QQ 모델 기반으로 정의되는 5가지 생리학적 파라미터(S0, R2, Y, v, χnb)가 포함되어 있으며, 이를 기반으로 모델의 입력 및 출력을 구성하였다.
제안한 커스텀 3D CNN 모델은 MRI로부터 획득한 3차원 구조 데이터를 중심으로 하여, 효과적인 학습과 메모리 효율을 동시에 확보할 수 있도록 입력 데이터를 제한된 관심 영역(ROI, Region of Interest) 내에서 크롭하여 활용하였다. 모델의 출력은 QQ 모델에서 정의된 다섯 가지 파라미터를 공간 단위로 예측하는 3차원 텐서로 구성되며, 이는 각 위치에서의 생리적 지표를 동시에 복원하는 회귀 문제로 정식화된다.
이러한 구조는 복수 채널 예측을 통해 단일 OEF 값과 관련된 Y 채널뿐만 아니라 관련 생리 변수 전체에 대한 정량적 추정을 가능하게 하며, 기존의 단일 채널 중심 예측 방식보다 더 정밀한 공간적 예측과 해석이 가능하다.
3.4 커스텀 3D CNN 모델 설계 전략
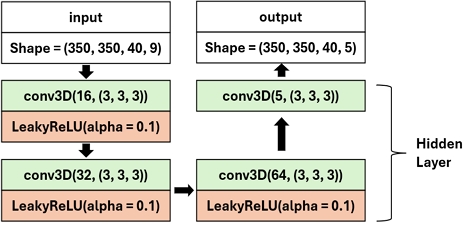
본 연구에서 제안한 모델은 기존 회귀 문제에서 높은 성능을 보이는 LSTM, ResNet, U-Net 등의 일반적인 구조를 사용하지 않고, Conv3D 연산과 활성화 함수만을 조합하여 설계된 커스텀 3D CNN 모델이다. 전체 구조는 단순하면서도 공간적 특징 학습에 최적화되어 있으며, 입력부터 출력까지 총 4개의 3D 합성곱 계층(Conv3D)으로 구성되어 있으며, 각 계층은 TE별 시그널과 자화율 정보를 포함하는 9채널의 3차원 볼륨 데이터를 받아들여 점진적으로 채널 수를 확장해 나가며 복잡한 공간 패턴을 학습하도록 구성되었다.
모델의 구조는 그림 2와 같이 입력 계층부터 출력 계층까지 순차적으로 연결된 형태로 이루어져 있으며, 각 은닉 계층에는 LeakyReLU 활성화 함수가 적용되어 음의 입력값에 대해서도 정보 손실을 최소화하도록 하였다. 입력 데이터는 (D×H×W) 해상도의 3차원 MRI 볼륨이다. 은닉 계층에서는 점진적으로 증가하는 채널 수와 함께 공간 정보를 효과적으로 압축하고, 최종 출력 계층에서는 QQ 모델의 생리 파라미터인 정맥 산소포화도(Y), 정맥 혈액량(v), 조직의 이완 계수(R2), 초기 신호 강도(S0), 자화율(χnb)에 해당하는 5채널의 출력을 생성한다.
Ⅳ. 실험 결과 및 분석
성능 검증을 위해 제안된 방법은 Intel i9-11900 CPU, Nvidia RTX 4090 GPU, 64GB RAM 하드웨어와 Windows 10 Pro 운영체제에서 PyTorch를 사용하여 구현하였다.
4.1 학습 설정 및 모델 선택
학습에 사용한 데이터셋은 코넬대학교 의과대학에서 구축한 MRI 데이터를 사용하였다. 해당 데이터셋은 총 17명의 환자에게서 수집된 3차원 뇌 MRI 신호 값과 자화율 데이터를 포함하며, QQ 모델에 사용되는 정맥 산소포화도, 정맥 혈액량, 조직의 가로 이완, TE 0에서 신호 강도, 비혈류 물질의 자화율에 대한 Ground Truth 값을 제공한다.
17명의 환자 데이터 중 학습을 위해 13명의 데이터를 활용하였으며, 나머지 4명의 데이터는 테스트를 위해 사용되었다.
기존 데이터는 512×512 (Width, Height) 크기로 불필요한 정보를 제거하기 위해서 중앙을 기준으로 350x350의 크기로 크롭하였고, 환자 데이터별 상이한 Slice 수와 초반 Slice, 후반 Slice의 경우 Mask를 활용하였을때 유의미하게 남는 정보가 없었기에 각 환자의 데이터마다 총 Slice의 중간을 기점으로 ±20으로 하여 40 Slice로 변형하였다. 이를 통해 모델의 학습에 있어서 컴퓨팅 자원 사용을 최소화하고 학습 속도와 정확도를 향상할 수 있게 하였다.
학습에서는 회귀 문제에서 예측 오차를 정량적으로 최소화하기 위해 평균 제곱 오차(MSE, Mean Squared Error)를 손실 함수로 설정하였으며, 최적화 알고리즘으로는 Adam을 사용하였다.
학습률은 초기값 0.001로 설정되었고, 학습률 조정에는 CosineAnnealingWarmupRestarts 스케줄러를 적용하였다. 이 스케줄러는 초반 100 스텝 동안 학습률을 선형적으로 증가시키는 Warm-up 단계를 거친 후, 코사인 함수에 따라 학습률을 점진적으로 감소시키는 구조로 되어 있으며, 첫 주기는 1,000 스텝, 이후 주기 길이는 고정(cycle_mult=1.0)되도록 구성하였다. 감쇠 계수는 0.9로 설정하여 학습 후반부의 미세 조정을 가능하게 하였다.
손실 계산에 있어서는 기존 연구들에서 흔히 적용해온 ROI 기반의 마스크 방식 대신, 전체 뇌 MRI 볼륨에 대해 손실을 평균화하는 전략을 채택하였다. 이를 통해 모델은 병변 외의 주변 조직과 배경까지 포함한 전반적인 공간적 특징을 학습할 수 있어, 특정 국소 영역에 대한 과적합을 방지하고 일반화 성능을 향상시키고자 하였다.
또한 학습 종료는 검증 손실(Validation loss)의 개선이 일정 기간 지속되지 않을 경우 조기 종료되도록 설계하였으며, patience 값은 적용한 학습 스케줄러의 2 cycle에 해당하는 2,000으로 설정하였다. 그 결과 총 28,958 epoch에서 조기 종료가 발생하였으며, 26,958 epoch에서 생성된 웨이트 값을 사용한다.
4.2 평가 정확도
학습에 사용하지 않은 테스트 데이터에 대하여 표 1은 QQ 모델을 구성하는 5개 생리학적 파라미터(S0, R2, Y, v, χnb)에 대해 기존의 DNN, 2D 기반 LSTM, 그리고 본 연구에서 제안한 커스텀 모델 간의 RMSE 값을 비교한 결과를 요약한 것이다.
제안한 모델은 Y 채널에서는 LSTM 방식에 비해 소폭 높은 오차를 보였지만, 나머지 네 개 채널에서는 가장 낮은 RMSE를 기록하여 전체적인 예측 안전성과 균형 측면에서 우수한 성능을 나타냈다.
특히 R2 채널에서는 기존 DNN 대비 약 60% 이상, LSTM 대비 약 14%의 RMSE 감소를 달성하였으며, 정맥혈액량(v)과 비혈류성 자화율(χnb)채널에서도 가장 낮은 오차를 보였다.
OEF 값은 다음 식 (2)를 통해서 계산할 수 있다. 여기서 Y는 정맥 산소포화도이며, Ya는 일반적으로 0.98로 설정되는 동맥 산소포화도이다. 이 값은 문헌 또는 생리학적 실험을 통해 정의되었고, 인체 내 정상적인 산소 포화 기준으로 사용된다.
| (2) |
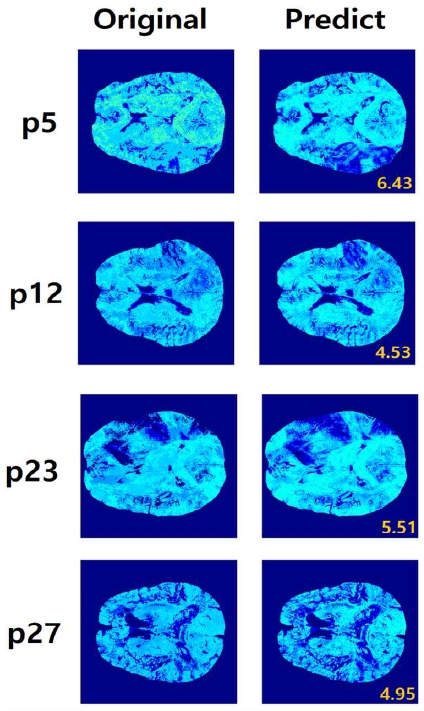
그림 3에는 해당 식 (2)을 바탕으로 제안한 모델을 통하여 OEF 예측 결과를 시각화하여 도시하였고, Ground Truth와 예측된 OEF 값 간의 정성적 일치도가 높음을 확인할 수 있다. 최종적으로 4개의 테스트 환자 데이터셋을 기반으로 계산된 평균 OEF RMSE는 5.39로, 기존 LSTM 방식의 5.33에 비하여 약간 높은 값을 기록하였다.
비록 OEF 예측 성능에서 기존의 2D LSTM 방식보다 다소 낮은 결과를 보였지만, 본 연구에서 제안한 커스텀 3D CNN 기반 모델은 나머지 파라미터에 대한 예측 성능이 향상되었으며, 전체적인 다채널 회귀 문제를 보다 균형있게 해결할 수 있는 구조임을 실험으로 입증하였다. 이는 임상적으로 다양한 지표를 동시에 고려해야 하는 상황에서 더욱 효과적으로 활용될 수 있음을 보인다.
Ⅴ. 결론 및 향후 과제
본 연구에서는 뇌 MRI 기반 OEF 예측의 정확도를 높이기 위해 커스텀 3차원 합성곱 신경망 구조를 설계하고, QQ 모델의 다섯 가지 주요 파라미터(S0, R2, Y, v, χnb)를 동시에 회귀 예측하는 딥러닝 기반 방법을 제안하였다. 제안한 모델은 자화율 및 TE별 신호 데이터를 포함한 4차원 입력을 3D CNN에 직접 적용함으로써 기존 2D 기반 접근보다 더욱 직관적이고 효율적인 구조를 확보하였다.
실험 결과, Y 채널에서는 약간 높은 RMSE를 기록하였으나, 나머지 네 개 채널(S0, R2, v, χnb)의 파라미터에 대해서는 전반적으로 향상된 예측 성능을 달성하였다. 이는 단일 채널 최적화가 아닌 다채널 회귀 문제에 대한 균형 잡힌 접근을 통해 전체 모델의 실용성과 일반화 가능성을 강화할 수 있음을 의미한다.
특히 ROI 마스킹 없이 전체 MRI 볼륨에 기반한 손실 함수 설계를 통해 국소 영역에 과도하게 의존하지 않고, 전반적인 뇌 조직 구조를 포괄적으로 학습함으로써 예측의 공간적 일관성과 안정성을 확보하였다. 이는 임상적으로 다양한 진단 요소를 함께 고려해야 하는 실제 환경에서 더욱 유의미한 결과를 제공할 수 있다.
제안한 방법은 QQ 모델 파라미터 예측의 정확성을 동시에 개선하였고 이를 통해 뇌 질환 진단 및 연구 분야에 실질적인 기여를 할 것으로 기대된다.
향후 연구에서는 손실 함수의 채널별 가중치 최적화, Y 채널 중심의 목적 함수 설계, 또는 하이브리드 구조의 적용을 통해 OEF 예측 성능을 더욱 향상할 수 있을 것으로 기대된다. 또한, 공개 데이터셋 활용, 3D 회전 및 노이즈 주입 등 데이터 다양성 확보를 위한 증강 기법 적용과 같은 추가적인 학습 데이터 확보 등을 통해 전반적인 예측 정확도와 일반화 성능을 동시에 개선할 수 있을 것이다.
Acknowledgments
This work was supported by the National Research Foundation of Korea(NRF) grant funded by the Korea government(MSIT) (No. RS-2023-00242116)
References
-
Y.-S. Hong and C.-P. Han, "Analysis for Heart Disease and Predictive Predictions Factor", The Journal of The Institute of Internet, Broadcasting and Communication, Vol. 24, No. 5, pp. 111-116, Oct. 2024.
[https://doi.org/10.7236/JIIBC.2024.24.5.111]

-
W. T. Kim and H. Y. Lee, "Prediction of Oxygen Extraction Fraction based on LSTM Deep Learning Model using Brain MRI", The Journal of Korean Institute of Information Technology, Vol. 22, No. 6, pp. 143-151, Jun. 2024.
[https://doi.org/10.14801/jkiit.2024.22.6.143]

-
H. S. Kim and H. Y. Lee, "DNN-based Oxygen Extraction Fraction Prediction Method for QQ Model of Brain MRI", The Journal of Korean Institute of Information Technology, Vol. 21, No. 6, pp. 35-41, Jun. 2023.
[https://doi.org/10.14801/jkiit.2023.21.6.35]

-
D. S. Bolar, B. R. Rosen, A. G. Sorensen, and E. Adalsteinsson, "QUantitative Imaging of eXtraction of oxygen and TIssue consumption (QUIXOTIC) using venular‐targeted velocity‐selective spin labeling", Magnetic Resonance in Medicine, Vol. 66, No. 6, pp. 1550-1562, Dec. 2011.
[https://doi.org/10.1002/mrm.22946]

-
X. He, M. Zhu, and D. A. Yablonskiy, "Validation of oxygen extraction fraction measurement by qBOLD technique", Magnetic Resonance in Medicine, Vol. 60, No. 4, pp. 882-888, Oct. 2008.
[https://doi.org/10.1002/mrm.21719]

-
Y. Wang and T. Liu, "Quantitative susceptibility mapping (QSM): decoding MRI data for a tissue magnetic biomarker", Magnetic Resonance in Medicine, Vol. 73, No. 1, pp. 82-101, Jan. 2015.
[https://doi.org/10.1002/mrm.25358]

-
J. Cho, Y. Kee, P. Spincemaille, T. D. Nguyen, J. Zhang, A. Gupta, S. Zhang, and Y. Wang, "Cerebral metabolic rate of oxygen (CMRO2) mapping by combining quantitative susceptibility mapping (QSM) and quantitative blood oxygenation level-dependent imaging (qBOLD)", Magnetic Resonance in Medicine, Vol. 80, No. 4, pp. 1595-1604, Oct. 2018.
[https://doi.org/10.1002/mrm.27135]

-
A. Alzaidi, H. Chappell, and D. Thomas, "Recent advances in quantitative BOLD (qBOLD) MRI: A scoping review of acquisition and clinical applications", Frontiers in Neuroscience, Vol. 18, pp. 1256872, Feb. 2024.
[https://doi.org/10.3389/fnins.2024.1256872]

-
T. T. Le, P. Bhogal, and K. T. Blockley, "Quantification of cerebral blood flow and oxygen extraction fraction using qBOLD MRI in response to acetazolamide-induced vasodilation", Magnetic Resonance in Medicine, Vol. 89, No. 6, pp. 2487-2502, Jun. 2023.
[https://doi.org/10.1002/mrm.29700]

-
Z. Feng, S. Liu, Y. Wang, and T. Liu, "MoDL-QSM: Model-based Deep Learning for Quantitative Susceptibility Mapping", Magnetic Resonance in Medicine, Vol. 86, No. 3, pp. 1901-1914, Sep. 2021.
[https://doi.org/10.1002/mrm.28829]

-
M. Cognolato, F. Zwartbol, B. Kasper, J. B. van Laarhoven, and A. Leemans, "NeXtQSM: A complete deep learning pipeline for robust quantitative susceptibility mapping", NeuroImage, Vol. 247, pp. 118823, Feb. 2022.
[https://doi.org/10.1016/j.neuroimage.2021.118823]

-
M. Zhang, L. Li, X. Zhou, and C. Liu, "INR-QSM: Implicit neural representation-based unsupervised quantitative susceptibility mapping", IEEE Transactions on Medical Imaging, Vol. 43, No. 2, pp. 345-356, Feb. 2024.
[https://doi.org/10.1109/TMI.2023.3345761]

-
Y. E. Seo, C. H. Son, and H. Y. Lee, "Method for Improving QQ-based Oxygen Extraction Fraction Estimation Accuracy through GRU Model", The Journal of Korean Institute of Information Technol ogy, Vol. 22, No. 7, pp. 131-139, Jul. 2024.
[https://doi.org/10.14801/jkiit.2024.22.7.131]

-
J. Cho, J. Zhang, P. Spincemaille, H. Zhang, S. Hubertus, Y. Wen, R. Jafari, S. Zhang, T. D. Nguyen, A. V. Dimov, A. Gupta, and Y. Wang, "QQ-NET – Using Deep Learning to Solve Quantitative Susceptibility Mapping and Quantitative Blood Oxygen Level Dependent Magnitude (QSM+qBOLD or QQ) Based Oxygen Extraction Fraction (OEF) Mapping", Magnetic Resonance in Medicine, Vol. 87, No. 3, pp. 1583-1594, Mar. 2022.
[https://doi.org/10.1002/mrm.29057]

-
Y. Chung, "Effects of Spatio-temporal Features of Dynamic Hand Gestures on Learning Accuracy in 3D-CNN", The Journal of The Institute of Internet, Broadcasting and Communication, Vol. 23, No. 3, pp. 145-151, Jun. 2023.
[https://doi.org/10.7236/JIIBC.2023.23.3.145]

- Z. Liu, "Super convergence cosine annealing with warm-up learning rate", Proc. of the 2nd International Conference on Artificial Intelligence, Big Data and Algorithms, Nanjing, China, pp. 1-7, Jun. 2022.
-
J. Cho, S. Zhang, Y. Kee, P. Spincemaille, T. D. Nguyen, S. Hubertus, A. Gupta, and Y. Wang, "Cluster analysis of time evolution (CAT) for quantitative susceptibility mapping (QSM) and quantitative blood oxygen level‐dependent magnitude (qBOLD)‐based oxygen extraction fraction (OEF) and cerebral metabolic rate of oxygen (CMRO2) mapping", Magnetic Resonance in Medicine, Vol. 83, pp. 844-857, Sep. 2019.
[https://doi.org/10.1002/mrm.27967]


2020년 3월 : 국립금오공과대학교 컴퓨터소프트웨어공학과 학사과정
관심분야 : Image Processing, Deep Learning

1997년 2월 : 성균관대학교 정보공학과(학사)
1999년 2월 : KAIST 전산학과(공학석사)
2006년 2월 : KAIST 전자전산학과(공학박사)
2008년 3월 ~ 현재 : 국립금오공과대학교 컴퓨터소프트웨어공학과 교수
관심분야 : Digital Forensics, Image Processing, IoT