뇌 MRI 신호 감쇠 모델링 기반 LSTM을 활용한 QQ 모델 파라미터 예측 및 OEF 추정
초록
뇌 질환의 조기 진단과 예후 관리를 위해 뇌에서 산소추출률(OEF)의 정밀한 추정은 중요하다. 기존 QQ 모델 기반 OEF 계산은 MRI 촬영 조건, 특히 에코 타임(TE)에 민감하다는 한계를 가진다. 본 연구에서는 mGRE 신호 감쇠를 지수 함수로 모델링하여 촬영 조건에 무관한 일반화 파라미터를 추정하고, 자화율 정보를 포함한 시퀀스를 구성하였다. 이를 LSTM 기반 딥러닝 모델에 입력함으로써 QQ 모델의 5개 입력 파라미터를 예측한 후 OEF를 산출하는 방법을 제안하였다. 18명의 환자 데이터를 이용한 실험에서 제안한 방법은 기존 클러스터링 기반의 CCM 방법에 비해 정맥 산소화를 포함한 일부 파라미터의 예측 오차를 감소시켰으며, OEF RMSE는 약 0.12 감소한 5.23±0.035로 나타났다. 이는 촬영 조건 변화에 대한 강건한 추정 가능성을 제시한다.
Abstract
Accurate estimation of the Oxygen Extraction Fraction (OEF) in the brain is essential for the early diagnosis and prognosis of brain disorders. Conventional QQ model-based OEF estimation is highly sensitive to Magnetic Resonance Imaging (MRI) acquisition parameters, particularly Echo Time (TE). In this study, mGRE signal decay was modeled using an exponential function to estimate generalized parameters independent of acquisition conditions, and a sequence was constructed incorporating susceptibility. By inputting this sequence into an LSTM-based deep learning model, we proposed a method to predict the five input parameters of the QQ model and subsequently estimate OEF. Experiments on MRI data from 18 patients demonstrated reduced prediction errors for several parameters, including venous oxygenation, compared with a conventional clustering-based CCM approach. The OEF RMSE decreased by approximately 0.12, reaching 5.23 ± 0.035, indicating robustness to variations in MRI acquisition conditions.
Keywords:
oxygen extraction fraction, brain MRI, QQ model, signal decay modeling, long short-term memory modelⅠ. 서 론
뇌 질환은 현대 사회에서 높은 사망률을 보이는 주요 건강 문제로, 환자의 예후를 개선하기 위해서는 조기 진단과 정밀한 검사가 필수적이다. 이를 위해 자기공명영상(MRI, Magnetic Resonance Imaging)이나 컴퓨터 단층촬영(CT, Computed Tomography)과 같은 비침습적 영상 기법이 활용되며, 뇌 조직의 상태를 반영하는 생리학적 정보를 획득할 수 있다. 특히 혈액으로부터 공급된 산소 중 뇌 조직이 실제로 소모한 비율을 나타내는 산소추출률(OEF, Oxygen Extraction Fraction)은 뇌 조직의 대사 및 기능적 상태를 정량적으로 평가하는 핵심 지표로, OEF를 정확하게 추정하기 위한 다양한 연구가 지속적으로 수행되고 있다.
대표적인 OEF 추정 기법으로는 QUIXOTIC(QUantitative Imaging of eXtraction of Oxygen and Tissue Consumption)[1], Calibrated fMRI[2], qBOLD(quantitative Blood Oxygenation Level Dependent)[3], 그리고 QSM(Quantitative Susceptibility Mapping)과 qBOLD 모델을 결합한 QQ(QSM+qBOLD) 모델[4][5] 등이 있다. 이들 중에서 QQ 모델은 특정 가정에 크게 의존하지 않으면서도 효율적인 OEF 예측이 가능하다는 장점으로 인해, 클러스터 기반 분석 및 딥러닝 기법과 결합된 연구가 활발히 수행되고 있다[6]-[10]. 그러나, 기존 QQ 모델 기반 연구들은 에코 타임(TE, Echo Time) 등 MRI 촬영 설정에 대한 의존도가 높고, MRI 신호에 포함된 잡음에 민감하다는 한계를 가진다[4][5]. 일부 연구에서는 잡음 환경에서도 보다 안정적인 OEF 예측 방법이 제안되었으나, 촬영 설정에 대한 의존성을 근본적으로 해소하는 데에는 여전히 한계가 존재한다[5][6]. 이러한 문제를 극복하기 위해 뇌 MRI 신호의 감쇠 특성을 지수 함수 형태로 일반화한 모델 파라미터를 기반으로 OEF를 예측하는 접근 방법이 제시되었다[11].
본 연구에서는 MRI 촬영 설정, 특히 TE에 대한 의존성을 완화하고 QQ 모델 파라미터를 정밀하게 예측하기 위해, MRI 신호 감쇠 모델링[11]과 LSTM(Long Short-Term Memory) 기반 딥러닝 구조를 결합한 예측 방법을 제안한다. 먼저 mGRE 시퀀스에서 획득한 신호를 MRI 신호 감쇠 모델링을 통해 일반화된 파라미터로 변환한다. 이를 시퀀스 형태의 입력 데이터로 구성하여 LSTM 계층에 전달함으로써, 비교적 짧은 에코 시퀀스 내에서도 신호 간의 시간적 상관관계를 효과적으로 학습할 수 있도록 설계하였다. 이를 통해 기존 QQ 모델 기반 방법들이 갖는 촬영 설정 의존성과 잡음 민감도 문제를 완화하고, 다양한 촬영 조건에서도 안정적인 QQ 모델 파라미터 예측 가능성을 확인하고자 한다.
본 논문의 구성은 다음과 같다. 2장에서는 관련 연구를 요약하고, 3장에서는 신호 감쇠 모델링 기반 LSTM 모델을 이용한 QQ 모델 파라미터 및 OEF 예측 방법을 설명한다. 4장에서는 실험 및 분석 결과를 제시하며, 5장에서는 결론을 제시한다.
Ⅱ. 관련 연구
2.1 QQ 모델 및 OEF 계산
위상 신호 기반 QSM 모델은 정맥 내 디옥시헤모글로빈에 의해 발생하는 자화율 변화와 비혈액 조직의 자화율 성분을 반영할 수 있다. 반면, 신호 세기 기반 qBOLD 모델은 mGRE(multi-echo gradient-echo) 시퀀스에서 획득된 MRI 신호 세기를 이용하여 OEF에 따른 신호 감쇠 효과를 모델링한다. 그러나 두 모델을 개별적으로 적용할 경우, qBOLD 모델에서는 비혈액 조직 자화율에 대한 가정이 필요하며, QSM 모델에서는 혈류량과 자화율 간의 관계에 대한 가정이 요구된다는 제약이 존재한다.
이러한 한계를 보완하기 위해 QQ 모델은 식 (1)과 같이 정의되며, QSM의 위상 정보와 qBOLD의 신호 세기 정보를 결합함으로써 각 모델에서 요구되는 파라미터들을 상호보완적으로 활용한다[4].
| (1) |
여기서 Y는 정맥 산소화, v는 정맥 혈액량을 의미한다. 또한, R2는 BOLD 효과가 없는 조직의 가로 방향 이완을 나타낸다. S0는 TE=0에서의 신호 세기를 의미하고, χnb는 비혈류 물질의 자화율(Non-blood susceptibility)을 나타낸다. 한편, w는 QSM 가중치를, λ는 정규화 가중치를 의미하며, FQSM 모델과 SqBOLD 모델에 대한 자세한 내용은 J. Cho et al.[5]와 H. Y. Lee[6]의 연구에 기술되어 있다.
OEF는 식 (2)와 같이 정맥 산소화 Y를 이용하여 계산된다. 여기서 Ya는 동맥 산소화 값으로, 보통 0.98로 가정된다. 이는 동맥의 산소화 상태에 대한 실험적 측정 결과를 기반으로 한 값이다[5].
| (2) |
2.2 MRI 신호 감쇠 모델링 기반 CCM 방법
기존 OEF 추정 방법들은 MRI 촬영을 위한 TE에 의존적인 한계를 가진다. 이를 보완하기 위해, Lee는 MRI 신호 감쇠 모델링을 통해 QQ 모델의 출력값을 일반화하고, 이를 기존의 클러스터 기반 방식과 결합한 OEF 계산 방법을 제안하였다[11].
해당 방법에서는 MRI 신호 감쇠에 대한 모델을 통하여 다양한 출력값을 (A, B, E)의 세 가지 간소화된 파라미터로 표현하였다. 각 파라미터를 계산하는 방법은 3.2절에서 설명한다.
이후 다양한 샘플로부터 신호 감쇠 모델링을 통해 추정된 파라미터를 대표 클러스터 데이터베이스와 정합하여 유사한 클러스터를 찾아내고, 보간을 통해 OEF를 계산한다. 실험 결과에 따르면 클러스터 데이터베이스 생성 시 사용한 조건과 다른 TE 및 에코 샘플수를 적용하였음에도 불구하고 OEF에 대한 RMSE 값이 유사하게 추정되어, MRI 촬영 조건 변화에 대해 일반화 성능과 효율성을 갖는 것을 확인하였다.
Ⅲ. 신호 감쇠 모델링을 통한 LSTM 기반 QQ 모델 파라미터 및 OEF 예측 방법
본 절에서는 MRI 촬영 설정에 대한 의존성을 최소화하면서 빠르고 정확한 QQ 모델 파라미터 추정 및 OEF을 위해, H. Y. Lee[11]에서 제안한 뇌 MRI 신호 감쇠 모델링을 기반으로 QQ 모델의 출력을 일반화하고 LSTM 기반 딥러닝 모델로 QQ 모델 파라미터를 추정한 뒤 이를 바탕으로 OEF를 산출하는 방법을 제안한다.
3.1 LSTM
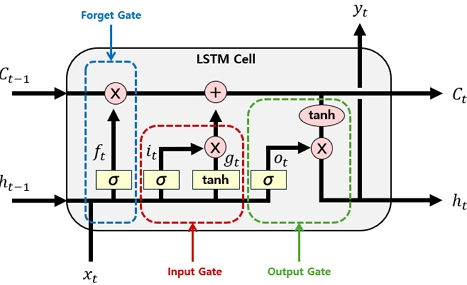
LSTM은 RNN(Recurrent Neural Network)의 한 종류로, 기존 RNN이 학습 과정에서 겪는 장기 의존성 문제를 완화하기 위해 제안된 모델이다[12]. LSTM은 그림 1과 같이 정보를 장기간 보관할 수 있는 셀 상태(Cell state)와 이를 제어하는 세 개의 게이트로 구성되며, 이를 통해 장기 및 단기 의존 정보를 효과적으로 관리한다.
LSTM의 은닉 상태 갱신 과정은 입력 게이트(Input gate), 망각 게이트(Forget gate), 출력 게이트(Output gate)에 의해 제어된다. 입력 게이트는 현재 입력으로부터 셀 상태에 반영할 정보를 결정하며, 망각 게이트는 이전 셀 상태 중 유지하거나 삭제할 정보를 선택한다. 이러한 두 결과를 결합하여 셀 상태를 갱신한 후, 출력 게이트는 셀 상태 중 다음 시점의 은닉 상태에 반영할 정보를 결정한다. 이와 같은 게이트 기반 구조를 통해 LSTM은 불필요한 정보는 제거하고 중요한 정보는 장기간 유지할 수 있으며, 그 결과 기울기 소실 문제를 완화하면서 장기 의존성을 효과적으로 학습할 수 있다.
3.2 MRI 신호 감쇠 모델링
자기공명영상(MRI)는 강한 자기장 환경에서 고주파 자극을 통해 수소 원자핵을 공명시킨 후, 원자핵의 자화가 안정 상태로 이완되는 과정에서 발생하는 신호를 측정하여 영상을 재구성하는 기법이다. mGRE 시퀀스에서는 서로 다른 TE에서 반복적으로 신호를 획득하며, 이때 관측되는 신호 세기는 잡음의 영향을 받는다. 또한 자기공명 특성상 TE가 증가함에 따라 신호 세기는 지수 함수 형태로 감소하는 경향을 보인다.
이러한 특성으로 인해 동일한 조직 조건에서도 TE 설정이나 에코 샘플링 조건에 따라 관측되는 신호 값이 달라질 수 있으며, 이는 mGRE 신호를 직접 활용하는 기존 QQ 모델 기반 분석에서 촬영 설정 의존성을 증가시키는 원인이 된다. 이러한 문제를 해결하기 위해 mGRE 시퀀스에서 획득한 신호의 감쇠 경향을 식 (3)과 같이 지수 함수 형태로 모델링하여, 다양한 촬영 환경에서도 일관된 표현이 가능한 신호 감쇠 모델링 기법이 제안되었다[11].
| (3) |
여기서 A는 지수 함수의 계수, B는 지수 가중치를 의미한다. E는 식 (4)와 같이 실제로 측정된 mGRE 시퀀스 출력값 M과 모델링된 신호값 사이의 평균 제곱근 오차(RMSE, Root Mean Square Error)를 나타낸다.
| (4) |
이와 같은 신호 감쇠 모델링을 적용함으로써, 서로 다른 TE 값이나 에코 개수를 사용하여 획득된 mGRE 신호를 세 개의 파라미터 (A, B, E)로 표현할 수 있다. 결과적으로 이는 촬영 설정에 대한 의존성을 완화하며, 이후 QQ 모델 출력값을 보다 일반화된 형태로 표현하는 기반을 제공한다.
3.3 LSTM 딥러닝 모델의 구조
본 논문에서 제안하는 LSTM 기반 딥러닝 모델은 MRI 신호 감쇠 모델링으로 추정한 3개의 파라미터(A, B, E)와 자화율(S)을 입력되는 특징으로 사용한다. 시간적 의존성을 반영하기 위해 각 샘플은 [A, B, E, S]로 구성된 4차원 특징 벡터를 5개 타임 스텝으로 배열한 시퀀스 형태로 입력되며, LSTM 계층은 이 시퀀스로부터 시점 간 상관관계와 변화 양상을 학습한다. 시퀀스 길이는 연산 효율성과 시간적 특징 반영 간의 균형을 고려하여 5로 설정하였다.
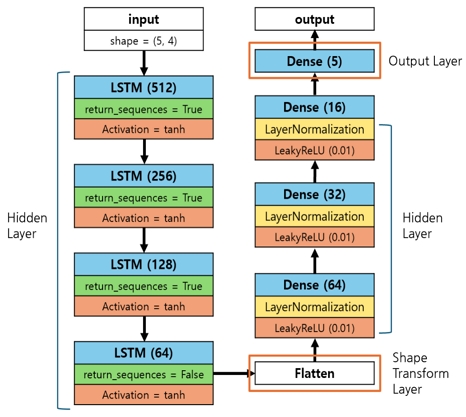
은닉 계층은 총 4개의 LSTM 계층으로 구성되며, 각 계층의 유닛 수는 512, 256, 128, 64로 점진적으로 감소하도록 설계하였다. 입력 이후 첫 3개의 LSTM 계층은 모든 타임 스텝의 출력을 다음 계층으로 전달하여 시퀀스 정보를 유지하도록 하였다. 반면 마지막 LSTM 계층에서는 최종 타임 스텝의 출력만 반환하여, 시퀀스 전체를 대표하는 단일 출력 벡터를 생성하였다. 이후 flatten 계층을 배치함으로써 뒤따르는 Dense 계층의 학습 안정성을 높였으며, flatten 계층을 거친 벡터를 입력으로 하여 총 3개의 Dense 블록을 순차적으로 적용하였다. 각 Dense 블록은 Dense, LayerNormalization, LeakyReLU 순으로 구성하여 학습 안정성과 비선형 표현력을 확보하였으며, Dense 계층의 유닛 수를 단계적으로 감소시키는 방식으로 다층 구조를 형성하였다.
각 은닉 블록에 대해서 배치 크기와 무관하게 개별 샘플의 특징 차원에서 정규화를 수행하는 LayerNormalization을 적용하였다. 이는 물리적 의미를 갖는 입력 특징으로부터 도출된 LSTM 출력 벡터를 처리하는 과정에서, 배치 전체의 통계량에 의존하는 BatchNormalization보다 샘플 내부 특징 간의 상대적 관계를 보존하는 데 더 적합하다고 판단하였기 때문이다. 또한, LeakyReLU 활성화 함수에 앞서 정규화를 진행하여 Dense 계층에서의 특성 분포를 안정함으로써, LSTM 이후 단계의 학습을 안정적으로 수행하고 최종 예측 정밀도를 향상시키고자 하였다.
활성화 함수로는 표준 LSTM 구성에 따라 LSTM 계층에서는 tanh를 사용하여 시점 간 정보를 비선형적으로 표현하도록 하였으며, Dense 계층에서는 기울기 소실 문제를 완화하기 위해 LeakyReLU를 적용하였다. LeakyReLU는 음의 입력값에 대해서도 작은 기울기를 유지함으로써 활성화 함수의 출력이 0에 고정되는 현상을 완화하고 네트워크의 비선형 학습 능력을 향상시킨다.
최종 출력 계층은 QQ 모델의 입력 파라미터에 해당하는 정맥 산소화(Y), 정맥 혈액량(v), 조직의 가로 이완(R2), TE=0에서의 신호 세기(S0), 비혈류 물질의 자화율(χnb)에 대응하는 5개 노드로 구성된다. 본 모델은 MRI 신호 감쇠 특성과 자화율 정보를 시퀀스 형태로 학습함으로써, 기존 방법 대비 촬영 설정 변화에 강인한 QQ 모델 파라미터 예측이 가능하도록 설계되었다. 전체 LSTM 기반 딥러닝 모델 구조는 그림 2에 제시하였다.
Ⅳ. 실험 결과 및 분석
본 연구에서 제안한 방법은 Intel i7-7700 CPU, NVIDIA RTX 3090, 32GB RAM 하드웨어 및 Window 10 Pro 운영체제에서 Tensorflow의 Keras로 구현하였고, 실험 및 성능 평가를 수행하였다.
4.1 데이터 획득 및 처리
본 연구에서는 코넬대학교 의과대학의 CAT 방법에서 사용된 것과 동일한 데이터셋을 활용하였다. 해당 데이터셋은 18명의 환자로부터 수집한 3차원 뇌 MRI 신호 및 자화율 데이터로 구성되며, 이에 대응하는 QQ 모델의 정맥 산소화, 정맥 혈액량, 조직의 가로 이완, TE=0에서의 신호 강도, 비혈류 물질의 자화율에 대한 Ground Truth 값을 포함한다[5][6].
MRI 촬영으로 획득한 3차원 뇌 MRI 데이터에서 각 복셀의 mGRE 신호를 TE 축에 따라 신호 감쇠 모델로 모델링하여 파라미터 A, B, E 및 자화율 S를 추정하였다. 이후 추정된 특징들을 학습에 활용하기 위해 3차원 데이터를 1차원으로 선형화하고, 시간적 정보를 반영할 수 있도록 타임 스텝이 5인 시퀀스 데이터로 전처리하여 모델 입력으로 사용하였다.
4.2 학습과 검증 정확도
제안한 LSTM 딥러닝 모델의 학습을 위해 전처리된 데이터를 학습, 검증 및 평가용으로 분할하여 사용하였다. 전체 18명 중 8명(P3, P4, P5, P14, P16, P28, P29, P34)의 데이터를 학습 및 검증에 활용하였으며, 이때, Train : Validation 비율은 8 : 2로 설정하였다. 나머지 10명의 환자 데이터는 모델의 성능 평가를 위해 사용하였다.
LSTM 모델의 학습률은 1e-4로 설정하였으며, 배치 크기는 512를 적용하였다. 손실 함수로는 Huber 손실을, 최적화 함수로는 Adam을 사용하였으며, 성능 평가지표로는 평균 제곱근 오차(RMSE)를 적용하였다. 학습은 최대 100 epoch까지 진행하되, 검증 데이터의 손실이 10 epoch 동안 감소하지 않을 경우, 조기 종료(Early stopping)되도록 설정하여 과적합을 방지하고 학습 효율성을 향상시켰다.
본 연구에서는 모델의 통계적 안정성을 평가하기 위해 데이터 분할을 고정하고 난수 시드(Random seed)만 변경하여 총 5회 독립 반복 실험을 수행하였다. 각 실험에서 평가 데이터에 대한 RMSE를 산출하여, 그 평균과 표준편차를 계산하였다.
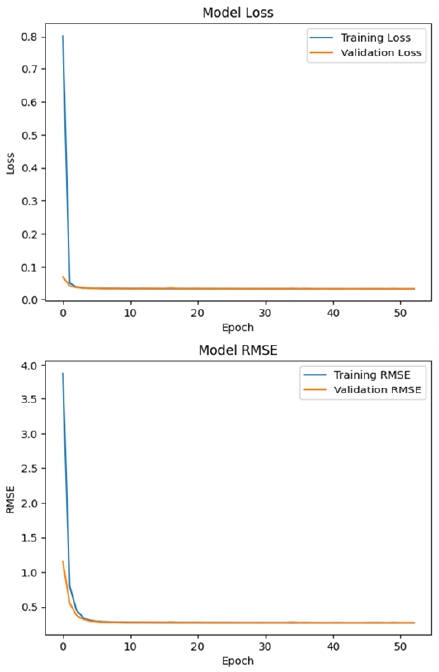
그림 3은 5회 반복 실험 중 전체 평균 RMSE와의 절대 차이가 가장 작은 실험을 대표 실험으로 선정하여, epoch에 따른 OEF 예측 RMSE와 손실 함수 값의 변화를 나타낸다. 그림에서 확인할 수 있듯이, RMSE와 손실 값은 학습이 진행됨에 따라 점진적으로 감소하다가 일정 시점 이후 수렴하는 경향을 보인다. 모델의 학습은 52 epoch 시점에서 조기 종료되었으며, 43 epoch에서 손실 값은 0.03397으로 최소값을 기록하였고, RMSE 또한 0.2710로 가장 낮은 오차를 보여 최적의 예측 성능을 보였다.
4.3 평가 정확도
제안한 LSTM 모델의 성능 평가는 학습 및 검증에 사용하지 않은 10명의 환자 데이터를 이용하여 수행하였다. 모델의 출력은 QQ 모델의 5개 입력 파라미터로 구성되며, 여기에는 OEF 예측에 활용되는정맥 산소화(Y)를 포함한 주요 파라미터들이 포함된다. 모델이 예측한 QQ 모델 파라미터 및 OEF 값의 정확도를 평가하기 위해, 예측 결과와 Ground Truth 데이터를 비교하였으며, 성능 지표로는 두 데이터 간의 평균 RMSE를 사용하였다.
표 1에는 상기 기준에 따라 선정된 대표 실험의 RMSE 값을 제시하였으며, 표 2에는 기존 클러스터링 기반 CCM 방법[11]과 제안한 방법의 성능을 비교하여 나타내었다. 제안한 방법의 성능은 5회 반복 실험에 대한 평균 ± 표준편차로 제시하였다.
실험 결과, 제안한 방법은 기존 클러스터링 기반 CCM 방법[11]에 비해 TE=0에서의 신호 세기(S0), 정맥 산소화(Y), 비혈류 물질의 자화율(χnb)에 대해 상대적으로 낮은 예측 오차를 보였다. 또한 5회 반복 실험에서 산출된 표준편차는 평균 대비 약 7% 이하로 나타나, 제안한 방법이 초기화(Random seed)에 유의한 영향을 받지 않으며 예측 성능의 변동이 제한적임을 확인하였다. 반면, 나머지 두 개의 파라미터, 특히 조직의 가로 이완(R2)에 대해서는 비교적 큰 오차가 발생함을 확인할 수 있었다.
일부 QQ 모델 파라미터에서 RMSE가 증가하는 한계가 존재하지만, 뇌 조직의 대사 상태 및 기능적 활성도를 평가하는 핵심 지표인 OEF 계산에 직접적으로 활용되는 Y 값의 예측 정확도가 향상되었다는 점에서 본 연구의 의의가 크다고 판단된다. 상대적으로 큰 오차가 나는 파라미터들(R2, v)에 대해서는 향후 모델 구조의 개선이나 파라미터 최적화 과정을 통해 보완이 가능할 것으로 보인다.
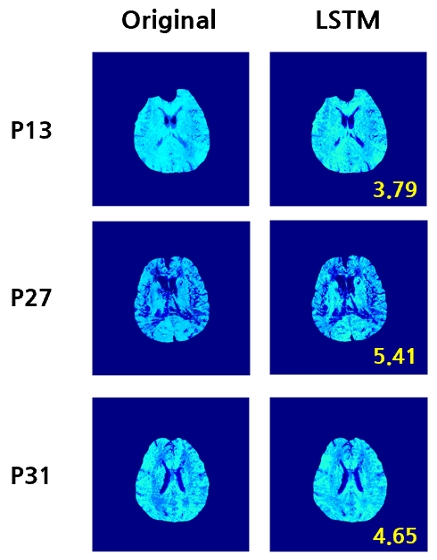
그림 4는 Ground Truth OEF 영상과 제안한 방법으로 추정한 OEF 영상을 시각적으로 비교한 결과를 도시하였다. 각 영상 우측에 표시된 노란색 숫자는 추정한 영상과 Ground Truth 간의 RMSE 값이다. 추정한 OEF 영상은 Ground Truth와 전반적으로 유사한 공간적 분포를 나타냈다. 이는 제안한 모델이 OEF 예측에서 유의미함을 시사한다.
표 3에는 기존의 클러스터링 방식과 제안한 방법의 OEF 예측 성능을 비교하였다. 제안한 방법의 OEF RMSE는 5.23±0.035로, CCM 방식[11]의 평균값 대비 약 0.12 감소하였다. 또한, 표준편차는 평균 대비 약 0.7% 수준으로 나타나 반복 실험 간 성능 변동이 제한적임이 확인되었다. 본 비교는 동일한 코넬대학교 의과대학의 데이터셋을 사용하여 수행되었으며, 학습 및 테스트 분할 비율에는 기존 연구와 일부 차이가 존재한다. 이러한 차이에도 불구하고, 제안한 모델은 QQ 모델 파라미터 및 OEF 예측에서 개선된 RMSE 성능과 안정적인 예측 특성을 나타냈다.
이와 같은 실험 결과를 통해, 뇌 MRI 신호에 대해 신호 감쇠 모델링을 적용함으로써 QQ 모델의 출력값을 일반화하고, 이를 기반으로 LSTM 기반 딥러닝 모델을 활용하여 QQ 모델의 5개의 입력 파라미터를 효율적으로 추정할 수 있음을 알 수 있다. 이는 제안한 LSTM 딥러닝 모델이 뇌 MRI 신호 분석에 있어서 기존 방법 대비 향상된 성능을 제공할 수 있음을 시사한다.
Ⅴ. 결론 및 향후 과제
뇌 질환 진단에 있어 뇌 조직 내 혈액의 산소 사용량을 정량적으로 평가하는 것은 뇌의 대사 상태와 활성화를 파악하고 정상 및 병리적 상태를 구분하는 데 중요한 임상적 지표가 된다. 이러한 과정에서 OEF 계산은 핵심적인 역할을 수행하며, OEF 계산에 직접적으로 사용되는 정맥 산소화(Y)를 포함한 QQ 모델 파라미터를 정확하게 예측하는 것은 여전히 중요한 연구 과제로 남아 있다.
OEF 계산을 위해 다양한 알고리즘이 제안되어 왔으며, 그중 QQ 모델은 특정 가정에 크게 의존하지 않으면서 효율적인 OEF 추정이 가능하다는 장점으로 인해 널리 활용되어 왔다. 그러나 QQ 모델은 TE와 같은 MRI 촬영 설정에 대한 의존성이 크다는 한계를 지니고 있다. 이를 보완하기 위해 mGRE 시퀀스 신호의 감쇠 특성을 지수 함수 형태로 모델링한 클러스터링 기반 접근 방법이 제안되었으나, 딥러닝을 활용한 연구는 아직 초기 단계에 머물러 있다.
본 연구에서는 QQ 모델 출력값을 일반화한 MRI 신호 감쇠 모델링을 기반으로 LSTM 딥러닝 모델을 설계하여, MRI 촬영 설정 변화에도 높은 정확도로 QQ 모델의 입력 파라미터를 추정하고 OEF를 예측하는 방법을 제안하였다. 18명의 환자 데이터를 이용한 실험 결과, 기존 클러스터링 기반 방법 대비 TE=0에서의 신호 세기(S0), 정맥 산소화(Y), 비혈류 물질의 자화율(χnb)에 대해 낮은 예측 오차를 보였으며, OEF 기준 RMSE를 약 0.12 감소시켜 5.23±0.035의 성능을 달성하였다. 이를 통해 본 연구는 OEF 계산의 정확도를 향상시키고, QQ 모델 파라미터 예측의 신뢰성을 개선할 수 있음을 확인하였다.
기존의 고정된 TE 신호를 기반으로 한 QQ 모델 파라미터 및 OEF 예측 방법과 달리, 본 연구는 뇌 MRI 신호의 감쇠 경향을 지수 함수로 모델링하여 일반화된 파라미터(A, B, E)와 자화율을 입력 특징으로 사용하였다. 또한 시간적 변화를 효과적으로 학습하기 위해 시퀀스 형태의 데이터를 LSTM 모델에 적용함으로써, 기존 클러스터링 기반 방법 대비 향상된 예측 성능을 달성하였다.
향후 연구에서는 조직의 가로 이완(R2)과 정맥 혈액량(v)에 대한 예측 정확도를 추가적으로 개선하기 위한 모델 구조 및 학습 전략의 고도화가 필요하다. 더 나아가, 보다 정밀한 뇌 질환 진단을 위해 본 연구에서 제안한 LSTM 기반 모델을 확장하여 성능이 향상된 다양한 딥러닝 모델 구조를 적용하는 연구가 요구된다.
Acknowledgments
This work was supported by the National Research Foundation of Korea(NRF) grant funded by the Korea government(MSIT) (No. RS-2023-00242116)
References
-
D. S. Bolar, B. R. Rosen, A. Sorensen, and E. Adalsteinsson, "Quantitative imaging of extraction of oxygen and tissue consumption (QUIXOTIC) using venular-targeted velocity-selective spin labeling", Magnetic Resonance in Medicine, Vol. 66, No. 6, pp. 1550-1562, Jun. 2011.
[https://doi.org/10.1002/mrm.22946]

-
R. G. Wise, A. D. Harris, A. J. Stone, and K. Murphy, "Measurement of OEF and absolute CMRO2: MRI-based methods using interleaved and combined hypercapnia and hyperoxia", NeuroImage, Vol. 83, pp. 135-147, Dec. 2013.
[https://doi.org/10.1016/j.neuroimage.2013.06.008]

-
X. He and D. A. Yablonskiy, "Quantitative BOLD: mapping of human cerebral deoxygenated blood volume and oxygen extraction fraction: default state", Magnetic Resonance in Medicine, Vol. 57, No. 1, pp. 115-126, Dec. 2006.
[https://doi.org/10.1002/mrm.21108]

-
J. Cho, Y. Kee, P. Spincemaille, T. D. Nguyen, J. Zhang, A. Gupta, S. Zhang, and Y. Wang, "Cerebral metabolic rate of oxygen (CMRO2) mapping by combining quantitative susceptibility mapping (QSM) and quantitative blood oxygenation level-dependent imaging (qBOLD)", Magnetic Resonance in Medicine, Vol. 80, No. 4, pp. 1595-1604, Mar. 2018.
[https://doi.org/10.1002/mrm.27135]

-
J. Cho, S. Zhang, Y. Kee, P. Spincemaille, T. D. Nguyen, S. Hubertus, A. Gupta, and Y. Wang, "Cluster analysis of time evolution (CAT) for quantitative susceptibility mapping (QSM) and quantitative blood oxygen level‐dependent magnitude (qBOLD)‐based oxygen extraction fraction (OEF) and cerebral metabolic rate of oxygen (CMRO2) mapping", Magnetic Resonance in Medicine, Vol. 83, pp. 844-857, Sep. 2019.
[https://doi.org/10.1002/mrm.27967]

-
H. Y. Lee, "OEF Calculation Method through Cluster-based Classification and Matching of QQ Model on Brain MRI Images", Journal of KIIT, Vol. 18, No. 10, pp. 15-23, Oct. 2020.
[https://doi.org/10.14801/jkiit.2020.18.10.15]

-
J. Cho, J. Zhang, P. Spincemaille, H. Zhang, S. Hubertus, Y. Wen, R. Jafari, S. Zhang, T. D. Nguyen, A. V. Dimov, A. Gupta, and Y. Wang, "QQ-NET - using deep learning to solve quantitative susceptibility mapping and quantitative blood oxygen level dependent magnitude (QSM+qBOLD or QQ) based oxygen extraction fraction (OEF) mapping", Magnetic Resonance in Medicine, Vol. 87, No. 3, pp. 1583-1594, Oct. 2021.
[https://doi.org/10.1002/mrm.29057]

-
S. Hubertus, S. Thomas, J. Cho, S. Zhang, Y. Wang, and L. R. Schad, "Using an artificial neural network for fast mapping of the oxygen extraction fraction with combined QSM and quantitative BOLD", Magnetic resonance in medicine, Vol. 82, No. 6, pp. 2199-2211, Jul. 2019.
[https://doi.org/10.1002/mrm.27882]

-
H. S. Kim and H.-Y. Lee, "DNN-based Oxygen Extraction Fraction Prediction Method for QQ Model of Brain MRI", The Journal of Korean Institute of Information Technology, Vol. 21, No. 6, pp. 35-41, Jun. 2023.
[https://doi.org/10.14801/jkiit.2023.21.6.35]

-
W. T. Kim and H.-Y. Lee, "Prediction of Oxygen Extraction Fraction based on LSTM Deep Learning Model using Brain MRI", The Journal of Korean Institute of Information Technology, Vol. 22, No. 6, pp. 143-151, Jun. 2024.
[https://doi.org/10.14801/jkiit.2024.22.6.143]

-
H. Y. Lee, "OEF Calculation Algorithm using Generalized QQ Model Clustering through Brain MRI Signal Decay Modeling", Journal of KIIT, Vol. 20, No. 5, pp. 1-8, May 2022.
[https://doi.org/10.14801/jkiit.2022.20.5.1]

-
S. Hochreiter and J. Schmidhuber, "Long Short-Term Memory", Neural Computation, Vol. 9, No. 8, pp. 1735-1780, Nov. 1997.
[https://doi.org/10.1162/neco.1997.9.8.1735]


2023년 3월 ~ 현재 : 국립금오공과대학교 컴퓨터소프트웨어공학과 학사과정
관심분야 : Computer Vision, Deep Learning

1997년 2월 : 성균관대학교 정보공학과(학사)
1999년 2월 : KAIST 전산학과(공학석사)
2006년 2월 : KAIST 전자전산학과(공학박사)
2008년 3월 ~ 현재 : 국립금오공과대학교 컴퓨터소프트웨어공학과 교수
관심분야 : Digital Forensics, Image Processing, Computer Vision, Internet of Things